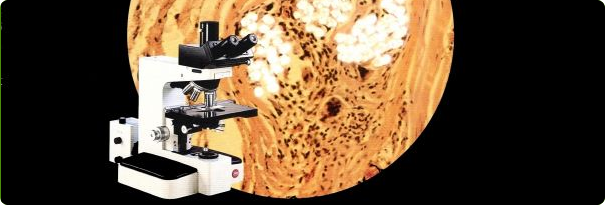
–¶–Є—В–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Њ–µ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П –њ–µ—А–Њ–Ї—Б–Є–і–∞–Ј—Л –≤ –ї–µ–є–Ї–Њ—Ж–Є—В–∞—Е.
–Я–µ—А–Њ–Ї—Б–Є–і–∞–Ј–љ–∞—П —А–µ–∞–Ї—Ж–Є—П (–Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Љ–Є–µ–ї–Њ–њ–µ—А–Њ–Ї—Б–Є–і–∞–Ј—Л –Ъ.–§. 1.11.1.7) –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –і–ї—П –≤—Л—П–≤–ї–µ–љ–Є—П –Љ–Є–µ–ї–Њ–Є–і–љ—Л—Е –Ї–ї–µ—В–Њ—З–љ—Л—Е —Н–ї–µ–Љ–µ–љ—В–Њ–≤. –Т–Љ–µ—Б—В–µ —Б –®–Ш–Ъ-—А–µ–∞–Ї—Ж–Є–µ–є –Є —А–µ–∞–Ї—Ж–Є–µ–є –љ–∞ –љ–µ—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї—Г—О —Н—Б—В–µ—А–∞–Ј—Г, –Љ–Є–µ–ї–Њ–њ–µ—А–Њ–Ї—Б–Є–і–∞–Ј–∞ —П–≤–ї—П–µ—В—Б—П –Њ–і–љ–Є–Љ –Є–Ј –Њ—Б–љ–Њ–≤–љ—Л—Е —Ж–Є—В–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е –Љ–µ—В–Њ–і–Њ–≤ –і–ї—П –і–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Њ—Б—В—А—Л—Е –ї–µ–є–Ї–Њ–Ј–Њ–≤.
–Я—А–Є–љ—Ж–Є–њ —А–µ–∞–Ї—Ж–Є–Є:
–Я–µ—А–Њ–Ї—Б–Є–і–∞–Ј–∞ —П–≤–ї—П–µ—В—Б—П —Д–µ—А–Љ–µ–љ—В–Њ–Љ - –ї–Є–Ј–Њ—Б–Њ–Љ–∞–ї—М–љ–Њ–є –Ї–∞—В–∞–ї–∞–Ј–Њ–є, –Ї–∞—В–∞–ї–Є–Ј–Є—А—Г—О—Й–µ–є –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є –њ–µ—А–µ–Ї–Є—Б–Є –≤–Њ–і–Њ—А–Њ–і–∞ –Њ–Ї–Є—Б–ї–µ–љ–Є–µ —А–∞–Ј–ї–Є—З–љ—Л—Е —Б—Г–±—Б—В—А–∞—В–Њ–≤. –Я—А–Є –Њ–Ї–Є—Б–ї–µ–љ–Є–Є –Њ—А—В–Њ—В–Њ–ї–Є–і–Є–љ–∞ –Є–ї–Є –±–µ–љ–Ј–Є–і–Є–љ–∞, –Є—Б–њ–Њ–ї—М–Ј—Г–µ–Љ—Л—Е –≤ —А–µ–∞–Ї—Ж–Є—П—Е, –Њ–±—А–∞–Ј—Г—О—В—Б—П –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ –Њ–Ї—А–∞—И–µ–љ–љ—Л–µ —Б–Њ–µ–і–Є–љ–µ–љ–Є—П, –≤ —В–Њ–Љ —Б–ї—Г—З–∞–µ, –µ—Б–ї–Є –≤ –Ї–ї–µ—В–Ї–µ –њ—А–Є—Б—Г—В—Б—В–≤—Г–µ—В –њ–µ—А–Њ–Ї—Б–Є–і–∞–Ј–∞, –њ—А–Є –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–Є —Б –Ї–Њ—В–Њ—А–Њ–є –њ–µ—А–µ–Ї–Є—Б—М –≤–Њ–і–Њ—А–Њ–і–∞ —А–∞–Ј—А—Г—И–∞–µ—В—Б—П —Б –≤—Л–і–µ–ї–µ–љ–Є–µ–Љ –Ї–Є—Б–ї–Њ—А–Њ–і–∞, –Ї–Њ—В–Њ—А—Л–є –Є –Њ–Ї–Є—Б–ї—П–µ—В –Њ—А—В–Њ-—В–Њ–ї–Є–і–Є–љ –Є–ї–Є –±–µ–љ–Ј–Є–і–Є–љ, –њ–µ—А–µ–≤–Њ–і—П –Є—Е –≤ –Њ–Ї—А–∞—И–µ–љ–љ—Л–µ —Б–Њ–µ–і–Є–љ–µ–љ–Є—П.
–†–µ–∞–≥–µ–љ—В—Л:
1.–С–µ–љ–Ј–Є–і–Є–љ
–†–µ–∞–Ї—В–Є–≤ –љ–∞ –њ–µ—А–Њ–Ї—Б–Є–і–∞–Ј—Г: –±–µ–љ–Ј–Є–і–Є–љ (–љ–∞ –Ї–Њ–љ—З–Є–Ї–µ –љ–Њ–ґ–∞) —А–∞—Б—В–≤–Њ—А—П—О—В –≤ 6 –Љ–ї 96 % —Б–њ–Є—А—В–∞, –њ—А–Є–±–∞–≤–ї—П—О—В 4 –Љ–ї –≤–Њ–і—Л –Є 0,02 –Љ–ї –Ч % –њ–µ—А–µ–Ї–Є—Б–Є –≤–Њ–і–Њ—А–Њ–і–∞. –†–µ–∞–Ї—В–Є–≤ –≥–Њ–і–µ–љ –Ї —Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є—О –≤ —В–µ—З–µ–љ–Є–µ 5вАФ6 –і–љ–µ–є
2.–Я–µ—А–µ–Ї–Є—Б—М –≤–Њ–і–Њ—А–Њ–і–∞ 3%.
3.–Ъ—А–∞—Б–Є—В–µ–ї—М –њ–Њ –†–Њ–Љ–∞–љ–Њ–≤—Б–Ї–Њ–Љ—Г..
4.–§–Є–Ї—Б–Є—А—Г—О—Й–∞—П —Б–Љ–µ—Б—М (10% —Б–њ–Є—А—В–Њ–≤–Њ–є —А–∞—Б—В–≤–Њ—А —Д–Њ—А–Љ–∞–ї–Є–љ–∞).–Я—А–Є–≥–Њ—В–Њ–≤–ї–µ–љ–Є–µ —Д–Є–Ї—Б–∞—В–Њ—А–∞ (10% —Б–њ–Є—А—В–Њ–≤–Њ–є —А–∞—Б—В–≤–Њ—А —Д–Њ—А–Љ–∞–ї–Є–љ–∞): 1–Љ–ї 40% —Д–Њ—А–Љ–∞–ї–Є–љ–∞ —Б–Љ–µ—И–Є–≤–∞—О—В —Б 9 –Љ–ї 96¬∞ —Н—В–Є–ї–Њ–≤–Њ–≥–Њ —Б–њ–Є—А—В–∞. –Ъ–∞–Ї –њ—А–Њ–Ј—А–∞—З–љ—Л–є, —В–∞–Ї –Є –Љ—Г—В–љ—Л–є –Љ–Њ–ї–Њ–Ї–Њ–Њ–±—А–∞–Ј–љ—Л–є —А–∞—Б—В–≤–Њ—А —Д–Њ—А–Љ–∞–ї–Є–љ–∞ –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ –њ—А–Є–≥–Њ–і–µ–љ. –Я–Њ–ї—Г—З–µ–љ–љ—Л–є 10% —А–∞—Б—В–≤–Њ—А —Д–Њ—А–Љ–∞–ї–Є–љ–∞ —Е—А–∞–љ–Є—В—Б—П –≤ —Е–Њ–ї–Њ–і–Є–ї—М–љ–Є–Ї–µ.
5. –Ф–Є—Б—В–Є–ї–ї–Є—А–Њ–≤–∞–љ–љ–∞—П –≤–Њ–і–∞;
6. 96¬∞ —Н—В–Є–ї–Њ–≤—Л–є —Б–њ–Є—А—В.
–Ю–±–Њ—А—Г–і–Њ–≤–∞–љ–Є–µ.
1. –°–µ–Ї—Г–љ–і–Њ–Љ–µ—А.
2. –°—В–µ–Ї–ї–∞ –њ—А–µ–і–Љ–µ—В–љ—Л–µ.
3. –†–µ–ї—М—Б—Л –Є–ї–Є –µ–Љ–Ї–Њ—Б—В–Є –і–ї—П –Њ–Ї—А–∞—Б–Ї–Є –Љ–∞–Ј–Ї–Њ–≤;
4. –Я–Є–њ–µ—В–Ї–Є
5. –Я—А–Њ–±–Є—А–Ї–Є —Е–Є–Љ.;
6. –С—Г–Љ–∞–≥–∞ —Д–Є–ї—М—В—А–Њ–≤–∞–ї—М–љ–∞—П;
7. –¶–Є–ї–Є–љ–і—А—Л –Љ–µ—А–љ—Л–µ –≤–Љ–µ—Б—В–Є–Љ–Њ—Б—В—М—О 25-500–Љ–ї.
8. –Я–µ—А—З–∞—В–Ї–Є —А–µ–Ј–Є–љ–Њ–≤—Л–µ
–Я–Њ–і–≥–Њ—В–Њ–≤–Ї–∞ –Ї –∞–љ–∞–ї–Є–Ј—Г.
–Я—А–Є–≥–Њ—В–Њ–≤–ї–µ–љ–Є–µ –Љ–∞–Ј–Ї–Њ–≤ –Ї—А–Њ–≤–Є –Є –Ї–Њ—Б—В–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞:
2-3 –Љ–∞–Ј–Ї–∞ –Ї—А–Њ–≤–Є (–Є–ї–Є –Ї–Њ—Б—В–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞) —Б–і–µ–ї–∞—В—М –љ–∞ –њ—А–µ–і–Љ–µ—В–љ—Л—Е —Б—В–µ–Ї–ї–∞—Е —Б –њ–Њ–Љ–Њ—Й—М—О –±–Њ–ї–µ–µ —Г–Ј–Ї–Њ–≥–Њ –њ—А–µ–і–Љ–µ—В–љ–Њ–≥–Њ —И–ї–Є—Д–Њ–≤–∞–љ–љ–Њ–≥–Њ —Б—В–µ–Ї–ї–∞ —Б–ї–µ–і—Г—О—Й–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ.
–Э–∞ —Б—Г—Е–Њ–µ –њ—А–µ–і–Љ–µ—В–љ–Њ–µ —Б—В–µ–Ї–ї–Њ, –±–ї–Є–ґ–µ –Ї –Ї–Њ—А–Њ—В–Ї–Њ–є —Б—В–Њ—А–Њ–љ–µ –љ–∞–љ–Њ—Б—П—В –њ–Є–њ–µ—В–Ї–Њ–є –љ–µ–±–Њ–ї—М—И—Г—О –Ї–∞–њ–ї—О –Ї—А–Њ–≤–Є. –Я—А–µ–і–Љ–µ—В–љ–Њ–µ —Б—В–µ–Ї–ї–Њ —Б–ї–µ–і—Г–µ—В –і–µ—А–ґ–∞—В—М –љ–∞ —Б—В–Њ–ї–µ –Є–ї–Є –≤ –ї–µ–≤–Њ–є —А—Г–Ї–µ –Ј–∞ —Г–Ј–Ї–Є–µ –Ї—А–∞—П. –Я—А–∞–≤–Њ–є —А—Г–Ї–Њ–є –њ—А–Є—Б—В–∞–≤–Є—В—М —И–ї–Є—Д–Њ–≤–∞–љ–љ–Њ–µ —Б—В–µ–Ї–ї–Њ —Г–Ј–Ї–Є–Љ –Ї—А–∞–µ–Љ –Ї —Б—В–µ–Ї–ї—Г —Б –Ї—А–Њ–≤—М—О —Б–ї–µ–≤–∞ –Њ—В –Ї–∞–њ–ї–Є –њ–Њ–і —Г–≥–ї–Њ–Љ –Љ–µ–љ–µ–µ 45¬∞ –Є –њ—А–Њ–і–≤–Є–љ—Г—В—М –µ–≥–Њ –≤–њ—А–∞–≤–Њ –і–Њ —Б–Њ–њ—А–Є–Ї–Њ—Б–љ–Њ–≤–µ–љ–Є—П —Б –Ї–∞–њ–ї–µ–є –Ї—А–Њ–≤–Є. –Т—Л–ґ–і–∞—В—М –і–Њ —В–µ—Е –њ–Њ—А, –њ–Њ–Ї–∞ –Ї—А–Њ–≤—М —А–∞—Б–њ–ї—Л–≤–µ—В—Б—П –њ–Њ –≤—Б–µ–Љ—Г —А–µ–±—А—Г —И–ї–Є—Д–Њ–≤–∞–љ–љ–Њ–≥–Њ —Б—В–µ–Ї–ї–∞, –Є –Ј–∞—В–µ–Љ –ї–µ–≥–Ї–Є–Љ –±—Л—Б—В—А—Л–Љ –і–≤–Є–ґ–µ–љ–Є–µ–Љ –њ—А–Њ–≤–µ—Б—В–Є –µ–≥–Њ —Б–њ—А–∞–≤–∞ –љ–∞–ї–µ–≤–Њ –і–Њ —В–µ—Е –њ–Њ—А, –њ–Њ–Ї–∞ –љ–µ –±—Г–і–µ—В –Є—Б—З–µ—А–њ–∞–љ–∞ –≤—Б—П –Ї–∞–њ–ї—П. –Ъ–∞–њ–ї—П –Ї—А–Њ–≤–Є –і–Њ–ї–ґ–љ–∞ –±—Л—В—М –љ–µ–±–Њ–ї—М—И–Њ–є –Є —Б–Њ—А–∞–Ј–Љ–µ—А–љ–∞ —В–∞–Ї, —З—В–Њ–±—Л –≤–µ—Б—М –Љ–∞–Ј–Њ–Ї –њ–Њ–Љ–µ—Й–∞–ї—Б—П –љ–∞ —Б—В–µ–Ї–ї–µ, –љ–µ –і–Њ—Е–Њ–і—П 1 - 1,5 —Б–Љ –і–Њ –µ–≥–Њ –Ї—А–∞—П. –Э–µ–ї—М–Ј—П —Б–Є–ї—М–љ–Њ –љ–∞–ґ–Є–Љ–∞—В—М –љ–∞ —Б—В–µ–Ї–ї–Њ, —В–∞–Ї –Ї–∞–Ї –Љ–љ–Њ–≥–Є–µ –Ї–ї–µ—В–Ї–Є –Ї—А–Њ–≤–Є –Љ–Њ–≥—Г—В –Њ–Ї–∞–Ј–∞—В—М—Б—П –њ–Њ–≤—А–µ–ґ–і–µ–љ–љ—Л–Љ–Є. –•–Њ—А–Њ—И–Њ —Б–і–µ–ї–∞–љ–љ—Л–є –Љ–∞–Ј–Њ–Ї —В–Њ–љ–Њ–Ї, –Є–Љ–µ–µ—В –ґ–µ–ї—В–Њ–≤–∞—В—Л–є —Ж–≤–µ—В –Є –Њ–Ї–∞–љ—З–Є–≤–∞–µ—В—Б—П вАЬ–Љ–µ—В–µ–ї–Њ—З–Ї–Њ–євАЭ.
–Я–Њ—Б–ї–µ –њ—А–Є–≥–Њ—В–Њ–≤–ї–µ–љ–Є—П –Љ–∞–Ј–Ї–Є —Б–ї–µ–і—Г–µ—В –±—Л—Б—В—А–Њ –≤—Л—Б—Г—И–Є—В—М –љ–∞ –≤–Њ–Ј–і—Г—Е–µ –і–Њ –Є—Б—З–µ–Ј–љ–Њ–≤–µ–љ–Є—П –≤–ї–∞–ґ–љ–Њ–≥–Њ –±–ї–µ—Б–Ї–∞. –Я—А–Є –Љ–µ–і–ї–µ–љ–љ–Њ–Љ –≤—Л—Б—Л—Е–∞–љ–Є–Є –Љ–Њ–ґ–µ—В –Є–Ј–Љ–µ–љ—П—В—М—Б—П –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—П –Ї–ї–µ—В–Њ–Ї –Ї—А–Њ–≤–Є
–Я—А–Є–≥–Њ—В–Њ–≤–ї–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Ї–Њ—Б—В–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ –∞–љ–∞–ї–Њ–≥–Є—З–љ–Њ –њ—А–Є–≥–Њ—В–Њ–≤–ї–µ–љ–Є—О –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –Ї—А–Њ–≤–Є.
–Я—А–Є–≥–Њ—В–Њ–≤–ї–µ–љ–Є–µ —А–∞–±–Њ—З–µ–≥–Њ —А–∞—Б—В–≤–Њ—А–∞:
–†–∞—Б—В–≤–Њ—А–Є—В—М —Б–Њ–і–µ—А–ґ–Є–Љ–Њ–µ –Њ–і–љ–Њ–≥–Њ —Д–ї–∞–Ї–Њ–љ–∞ –±–µ–љ–Ј–Є–і–Є–љ–∞ ( –Њ—А—В–Њ-—В–Њ–ї–Є–і–Є–љ–∞ ), –≤ 3–Љ–ї 96?—Н—В–Є–ї–Њ–≤–Њ–≥–Њ —Б–њ–Є—А—В–∞ –Є –і–Њ–ї–Є—В—М 2–Љ–ї –і–Є—Б—В–Є–ї–ї–Є—А–Њ–≤–∞–љ–љ–Њ–є –≤–Њ–і—Л. –•–Њ—А–Њ—И–Њ –≤–Ј–±–Њ–ї—В–∞—В—М –Є –њ–µ—А–µ–і —Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є–µ–Љ –і–Њ–±–∞–≤–Є—В—М –њ–Є–њ–µ—В–Ї–Њ–є 1 –Ї–∞–њ–ї—О 3% –њ–µ—А–µ–Ї–Є—Б–Є –≤–Њ–і–Њ—А–Њ–і–∞.
–•–Њ–і —А–µ–∞–Ї—Ж–Є–Є:
–°—Г—Е–Є–µ –Љ–∞–Ј–Ї–Є –Ї—А–Њ–≤–Є –Є–ї–Є –Ї /–Љ–Њ–Ј–≥–∞ —Д–Є–Ї—Б–Є—А–Њ–≤–∞—В—М –≤ 10% —Б–њ–Є—А—В - —Д–Њ—А–Љ–∞–ї–Є–љ–Њ–≤–Њ–є —Б–Љ–µ—Б–Є
| –љ–µ –±–Њ–ї–µ–µ 15—Б–µ–Ї—Г–љ–і!
| –Я—А–Њ–Љ—Л—В—М –њ—А–Њ—В–Њ—З–љ–Њ–є –≤–Њ–і–Њ–є
| 10—Б–µ–Ї.
| –°—В–µ–Ї–ї–∞ —Б –Љ–∞–Ј–Ї–∞–Љ–Є –Ї—А–Њ–≤–Є –Є–ї–Є –Ї–Њ—Б—В–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ –њ–Њ–Љ–µ—Б—В–Є—В—М –љ–∞ —А–µ–ї—М—Б—Л –Є –љ–∞ –љ–Є—Е –љ–∞–ї–Є—В—М —Б–≤–µ–ґ–µ–њ—А–Є–≥–Њ—В–Њ–≤–ї–µ–љ–љ—Л–є —А–∞–±–Њ—З–Є–є —А–∞—Б—В–≤–Њ—А —Б —В–Њ–ї—М–Ї–Њ —З—В–Њ –і–Њ–±–∞–≤–ї–µ–љ–љ–Њ–є –≤ –љ–µ–≥–Њ 3 %H2O2 –њ–µ—А–µ–Ї–Є—Б—М—О –≤–Њ–і–Њ—А–Њ–і–∞
–Я—А–Є–Љ–µ—З–∞–љ–Є–µ: –њ—А–Є –љ–∞–ї–Є—З–Є–Є –і–Њ—Б—В–∞—В–Њ—З–љ–Њ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –Љ–∞–Ј–Ї–Њ–≤ –Њ–Ї—А–∞—Б–Ї—Г –Љ–Њ–ґ–љ–Њ –њ—А–Њ–Є–Ј–≤–Њ–і–Є—В—М –≤ –µ–Љ–Ї–Њ—Б—В–Є –•–µ–ї–ї–µ–љ–і–∞—Е–µ–ї–∞ (8 –њ—А–µ–њ–∞—А–∞—В–Њ–≤) –Є–ї–Є –Ъ–Њ–њ–ї–Є–љ–∞ (5 –њ—А–µ–њ–∞—А–∞—В–Њ–≤).
–Я—А–Є —Н—В–Њ–Љ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ—А–Є–≥–Њ—В–Њ–≤–Є—В—М —А–∞–±–Њ—З–Є–є —А–∞—Б—В–≤–Њ—А –≤ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ, –і–Њ—Б—В–∞—В–Њ—З–љ–Њ–Љ –і–ї—П –Ј–∞–њ–Њ–ї–љ–µ–љ–Є—П –µ–Љ–Ї–Њ—Б—В–Є.
| –Ю—Б—В–∞–≤–Є—В—М –љ–∞ 15- 20–Љ–Є–љ –њ—А–Є –Ї–Њ–Љ–љ–∞—В–љ–Њ–є —В–µ–Љ–њ–µ—А–∞—В—Г—А–µ.
| –Я—А–Њ–Љ—Л—В—М –і–Є—Б—В–Є–ї–ї–Є—А–Њ–≤–∞–љ–љ–Њ–є –≤–Њ–і–Њ–є –Є –њ—А–Њ–Љ–Њ–Ї–љ—Г—В—М —Д–Є–ї—М—В—А–Њ–≤–∞–ї—М–љ–Њ–є –±—Г–Љ–∞–≥–Њ–є
| 10—Б–µ–Ї.
| –Ф–Њ–Ї—А–∞—Б–Є—В—М 0,5% —А–∞—Б—В–≤–Њ—А–Њ–Љ –Ї—А–∞—Б–Є—В–µ–ї—П –њ–Њ –†–Њ–Љ–∞–љ–Њ–≤—Б–Ї–Њ–Љ—Г
| 15-20–Љ–Є–љ.
| –Я—А–Њ–Љ—Л—В—М —Б—В–µ–Ї–ї–∞ –≤ –њ—А–Њ—В–Њ—З–љ–Њ–є –≤–Њ–і–µ
| 10—Б–µ–Ї
|
–Я—А–Є–Љ–µ—З–∞–љ–Є–µ:
–¶–Є—В–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ—А–Њ–≤–Њ–і—П—В –≤ –Љ–∞–Ј–Ї–∞—Е –Ї—А–Њ–≤–Є, –Ї–Њ—Б—В–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞, –ї–µ–є–Ї–Њ–Ї–Њ–љ—Ж–µ–љ—В—А–∞—В–∞, —Б–њ–Є–љ–љ–Њ–Љ–Њ–Ј–≥–Њ–≤–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є, –∞—Б–њ–Є—А–∞—В–∞—Е –ї–Є–Љ—Д–Њ—Г–Ј–ї–Њ–≤, —Б–µ–ї–µ–Ј–µ–љ–Ї–Є, –ї–µ–є–Ї–Њ–Ј–љ—Л—Е –Є–љ—Д–Є–ї—М—В—А–∞—В–∞—Е —А–∞–Ј–љ–Њ–є –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–Є.
–Ь–∞–Ј–Ї–Є –Ї—А–Њ–≤–Є –Є –Ї–Њ—Б—В–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ –ї—Г—З—И–µ –і–µ–ї–∞—В—М –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ –Є–Ј –Љ–∞—В–µ—А–Є–∞–ї–∞, –њ–Њ–ї—Г—З–µ–љ–љ–Њ–≥–Њ –±–µ–Ј –і–Њ–±–∞–≤–ї–µ–љ–Є—П –∞–љ—В–Є–Ї–Њ–∞–≥—Г–ї—П–љ—В–Њ–≤.
–Я—А–Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –ї–µ–є–Ї–Њ–њ–µ–љ–Є–Є —Ж–Є—В–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –њ—А–Њ–≤–Њ–і–Є—В—М –≤ –њ—А–µ–њ–∞—А–∞—В–∞—Е, –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е –Є–Ј –ї–µ–є–Ї–Њ–Ї–Њ–љ—Ж–µ–љ—В—А–∞—В–∞ –≤–µ–љ–Њ–Ј–љ–Њ–є –Ї—А–Њ–≤–Є.
–Я—А–Є–≥–Њ—В–Њ–≤–ї–µ–љ–љ—Л–µ –Љ–∞–Ј–Ї–Є –љ–µ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П —Е—А–∞–љ–Є—В—М –±–Њ–ї–µ–µ 24—З–∞—Б–Њ–≤, —В. –Ї. –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ—Л—Е —Д–µ—А–Љ–µ–љ—В–Њ–≤ —Б–љ–Є–ґ–∞–µ—В—Б—П.
–Э–µ—Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–љ—Л–µ –Љ–∞–Ј–Ї–Є –Љ–Њ–≥—Г—В —Е—А–∞–љ–Є—В—М—Б—П –≤ —В–µ–Љ–љ–Њ—В–µ –≤ —В–µ—З–µ–љ–Є–µ 3 –љ–µ–і–µ–ї—М.
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Њ–Ї—А–∞—Б–Ї–Є:
–Э–Њ—А–Љ–∞–ї—М–љ—Л–µ –≤–µ–ї–Є—З–Є–љ—Л:
–Т –Ї—А–Њ–≤–Є –Ј–і–Њ—А–Њ–≤—Л—Е –ї—О–і–µ–є 3- 16% –љ–µ–є—В—А–Њ—Д–Є–ї–Њ–≤ –Њ–Ї—А–∞—И–µ–љ—Л —А–µ–Ј–Ї–Њ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ, 60-90%- –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ, –Њ—Б—В–∞–ї—М–љ—Л–µ вАУ —Б–ї–∞–±–Њ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ. –°–¶–Ъ –љ–µ–є—В—А–Њ—Д–Є–ї–Њ–≤ –Ј–і–Њ—А–Њ–≤—Л—Е –ї—О–і–µ–є —А–∞–≤–µ–љ 2,56¬±0,033.
–Ш–Ј–Љ–µ–љ–µ–љ–Є—П –њ—А–Є –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–Њ—Б—В–Њ—П–љ–Є—П—Е
–†–µ–∞–Ї—Ж–Є—П –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –≥–ї–∞–≤–љ—Л–Љ –Њ–±—А–∞–Ј–Њ–Љ —Б —Ж–µ–ї—М—О –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Њ—Б—В—А—Л—Е –ї–µ–є–Ї–Њ–Ј–Њ–≤. –Я—А–Є –Њ—Б—В—А—Л—Е –Љ–Є–µ–ї–Њ–±–ї–∞—Б—В–љ—Л—Е –ї–µ–є–Ї–Њ–Ј–∞—Е –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —Д–µ—А–Љ–µ–љ—В–∞ –≤ –±–ї–∞—Б—В–∞—Е –≤–∞—А—М–Є—А—Г–µ—В –Њ—В —Г–Љ–µ—А–µ–љ–љ–Њ–є –і–Њ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є, –њ—А–Є –Њ—Б—В—А—Л—Е –Љ–Њ–љ–Њ–±–ї–∞—Б—В–љ—Л—Е- —Б–ї–∞–±–∞—П, –њ—А–Є –Њ—Б—В—А—Л—Е –ї–Є–Љ—Д–Њ–±–ї–∞—Б—В–љ—Л—Е вАУ –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ–∞—П.
–¶–Є—В–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Љ–Є–µ–ї–Њ–њ–µ—А–Њ–Ї—Б–Є–і–∞–Ј—Л
–Ь–Є–µ–ї–Њ–њ–µ—А–Њ–Ї—Б–Є–і–∞–Ј–∞ —П–≤–ї—П–µ—В—Б—П –ї–Є–Ј–Њ—Б–Њ–Љ–∞–ї—М–љ—Л–Љ —Д–µ—А–Љ–µ–љ—В–Њ–Љ, –Ї–∞—В–∞–ї–Є–Ј–Є—А—Г—О—Й–Є–Љ –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є –њ–µ—А–µ–Ї–Є—Б–Є –≤–Њ–і–Њ—А–Њ–і–∞ –Њ–Ї–Є—Б–ї–µ–љ–Є–µ —А–∞–Ј–ї–Є—З–љ—Л—Е —Б—Г–±—Б—В—А–∞—В–Њ–≤. –Ю–љ–∞ –ї–Њ–Ї–∞–ї–Є–Ј—Г–µ—В—Б—П –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –≤ —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є—Е –∞–Ј—Г—А–Њ—Д–Є–ї—М–љ—Л—Е –≥—А–∞–љ—Г–ї–∞—Е –≤ —Ж–Є—В–Њ–њ–ї–∞–Ј–Љ–µ –≥—А–∞–љ—Г–ї–Њ—Ж–Є—В–Њ–≤ –Є —П–≤–ї—П–µ—В—Б—П –Љ–∞—А–Ї–µ—А–Њ–Љ –Ї–ї–µ—В–Њ–Ї –Љ–Є–µ–ї–Њ–Є–і–љ–Њ–≥–Њ —А—П–і–∞. –Ь–Є–µ–ї–Њ–њ–µ—А–Њ–Ї—Б–Є–і–∞–Ј–∞ –≤—Л—П–≤–ї—П–µ—В—Б—П –≤ –Ї–ї–µ—В–Ї–∞—Е –≥—А–∞–љ—Г–ї–Њ—Ж–Є—В–∞—А–љ–Њ–≥–Њ —А—П–і–∞, –љ–∞—З–Є–љ–∞—П —Б –Љ–Є–µ–ї–Њ–±–ї–∞—Б—В–∞. –Р–Ї—В–Є–≤–љ–Њ—Б—В—М —Д–µ—А–Љ–µ–љ—В–∞ –њ–Њ–≤—Л—И–∞–µ—В—Б—П –њ–Њ –Љ–µ—А–µ —Б–Њ–Ј—А–µ–≤–∞–љ–Є—П –Ї–ї–µ—В–Њ–Ї. –Т —Б–µ–≥–Љ–µ–љ—В–Њ—П–і–µ—А–љ—Л—Е –љ–µ–є—В—А–Њ—Д–Є–ї–∞—Е –Ј–і–Њ—А–Њ–≤—Л—Е –ї—О–і–µ–є –≤—Л—П–≤–ї—П–µ—В—Б—П –≤—Л—Б–Њ–Ї–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Љ–Є–µ–ї–Њ–њ–µ—А–Њ–Ї—Б–Є–і–∞–Ј—Л –≤ –≤–Є–і–µ –≥—А–∞–љ—Г–ї, –Ј–∞–њ–Њ–ї–љ—П—О—Й–Є—Е —Ж–Є—В–Њ–њ–ї–∞–Ј–Љ—Г.
–°–∞–Љ–∞—П –≤—Л—Б–Њ–Ї–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —Д–µ—А–Љ–µ–љ—В–∞ –љ–∞–±–ї—О–і–∞–µ—В—Б—П –≤ –Ј—А–µ–ї—Л—Е —Н–Њ–Ј–Є–љ–Њ—Д–Є–ї–∞—Е. –Т –±–∞–Ј–Њ—Д–Є–ї—М–љ—Л—Е –њ—А–Њ–Љ–Є–µ–ї–Њ—Ж–Є—В–∞—Е –Є –Љ–Є–µ–ї–Њ—Ж–Є—В–∞—Е –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Љ–Є–µ–ї–Њ–њ–µ—А–Њ–Ї—Б–Є–і–∞–Ј—Л, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –≤—Л—Б–Њ–Ї–∞—П. –Ю–і–љ–∞–Ї–Њ, –њ–Њ –Љ–µ—А–µ –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–Ї–Є –Є—Е –≤ –Ј—А–µ–ї—Л–µ –Ї–ї–µ—В–Ї–Є, –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —Д–µ—А–Љ–µ–љ—В–∞ —Б–љ–Є–ґ–∞–µ—В—Б—П. –Ч—А–µ–ї—Л–µ –±–∞–Ј–Њ—Д–Є–ї—Л –Љ–Њ–≥—Г—В –±—Л—В—М –њ–Њ—З—В–Є –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–Љ–Є –њ–Њ –і–∞–љ–љ–Њ–Љ—Г –њ—А–Є–Ј–љ–∞–Ї—Г. –°–ї–∞–±–Њ–њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–∞—П —А–µ–∞–Ї—Ж–Є—П –љ–∞ –Љ–Є–µ–ї–Њ–њ–µ—А–Њ–Ї—Б–Є–і–∞–Ј—Г –љ–∞–±–ї—О–і–∞–µ—В—Б—П –≤ —А–∞–Ј–ї–Є—З–љ–Њ–Љ –њ—А–Њ—Ж–µ–љ—В–µ –Љ–Њ–љ–Њ—Ж–Є—В–Њ–≤ –≤ –≤–Є–і–µ –љ–µ–Љ–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л—Е —А–∞—Б—Б–µ—П–љ–љ—Л—Е –≥—А–∞–љ—Г–ї. –Т —Н—А–Є—В—А–Њ–Ї–∞—А–Є–Њ—Ж–Є—В–∞—Е, –ї–Є–Љ—Д–Њ—Ж–Є—В–∞—Е –Є –Љ–µ–≥–∞–Ї–∞—А–Є–Њ—Ж–Є—В–∞—Е –Љ–Є–µ–ї–Њ–њ–µ—А–Њ–Ї—Б–Є–і–∞–Ј–∞ –љ–µ –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П.
–Т –Ї–ї–µ—В–Ї–∞—Е –Љ–Є–µ–ї–Њ–њ–µ—А–Њ–Ї—Б–Є–і–∞–Ј–∞ —Г—З–∞—Б—В–≤—Г–µ—В –≤ —А–µ–∞–Ї—Ж–Є—П—Е —А–∞–Ј—А—Г—И–µ–љ–Є—П —В–Њ–Ї—Б–Є—З–љ–Њ–є –њ–µ—А–µ–Ї–Є—Б–Є –≤–Њ–і–Њ—А–Њ–і–∞. –Т —Ж–Є—В–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е —А–µ–∞–Ї—Ж–Є—П—Е –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —Д–µ—А–Љ–µ–љ—В–∞ –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П –њ–Њ –Њ–Ї–Є—Б–ї–µ–љ–Є—О —Е—А–Њ–Љ–Њ–≥–µ–љ–Њ–≤ (–±–µ–љ–Ј–Є–і–Є–љ–∞, –Њ-–і–Є–∞–љ–Є–Ј–Є–і–Є–љ–∞ –Є –і—А—Г–≥–Є—Е) –њ–Њ –Љ–µ—В–Њ–і—Г –У—А—Н—Е–µ–Љ–∞вАУ–Ъ–љ–Њ–ї–ї—П –Є–ї–Є –µ–≥–Њ –Љ–Њ–і–Є—Д–Є–Ї–∞—Ж–Є–є.
–Ь–µ—В–Њ–і –У—А—Н—Е–µ–Љ–∞-–Ъ–љ–Њ–ї–ї—П
–Я—А–Є–љ—Ж–Є–њ –Љ–µ—В–Њ–і–∞: –Т –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є –Љ–Є–µ–ї–Њ–њ–µ—А–Њ–Ї—Б–Є–і–∞–Ј—Л –±–µ–љ–Ј–Є–і–Є–љ –Њ–Ї–Є—Б–ї—П–µ—В—Б—П –њ–µ—А–µ–Ї–Є—Б—М—О –≤–Њ–і–Њ—А–Њ–і–∞ –≤ –Ї–Њ—А–Є—З–љ–µ–≤—Л–є –Њ–Ї—Б–Є–±–µ–љ–Ј–Є–і–Є–љ.
–Я–Њ—Б—Г–і–∞
* –•–Є–Љ–Є—З–µ—Б–Ї–Є–µ —Б—В–∞–Ї–∞–љ—Л.
* –Ь–µ—А–љ—Л–µ —Ж–Є–ї–Є–љ–і—А—Л.
* –Я–Є–њ–µ—В–Ї–Є.
–†–µ–∞–Ї—В–Є–≤—Л:
* 4% —Д–Њ—А–Љ–∞–ї–Є–љ–Њ–≤–Њ-—Б–њ–Є—А—В–Њ–≤–Њ–є —А–∞—Б—В–≤–Њ—А (10 —З–∞—Б—В–µ–є 40% —Д–Њ—А–Љ–∞–ї–Є–љ–∞ –Є 90 —З–∞—Б—В–µ–є 96% —Б–њ–Є—А—В–∞).
* –Я–µ—А–Њ–Ї—Б–Є–і–∞–Ј–љ—Л–є —А–µ–∞–Ї—В–Є–≤: –±–µ–љ–Ј–Є–і–Є–љ (–љ–∞ –Ї–Њ–љ—З–Є–Ї–µ –љ–Њ–ґ–∞) —А–∞—Б—В–≤–Њ—А—П—О—В –≤ 6 –Љ–ї 96% —Б–њ–Є—А—В–∞, –њ—А–Є–±–∞–≤–ї—П—О—В 4 –Љ–ї –≤–Њ–і—Л –Є 0,02 –Љ–ї 3% –њ–µ—А–µ–Ї–Є—Б–Є –≤–Њ–і–Њ—А–Њ–і–∞. –†–µ–∞–Ї—В–Є–≤ –≥–Њ–і–µ–љ –Ї —Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є—О –≤ —В–µ—З–µ–љ–Є–µ 5 вАФ 6 –і–љ–µ–є.
* –Ъ—А–∞—Б–Є—В–µ–ї—М –†–Њ–Љ–∞–љ–Њ–≤—Б–Ї–Њ–≥–Њ-–У–Є–Љ–Ј—Л.
–•–Њ–і –Њ–Ї—А–∞—Б–Ї–Є:
* –°–≤–µ–ґ–Є–µ –Љ–∞–Ј–Ї–Є (1-2-–і–љ–µ–≤–љ–Њ–є –і–∞–≤–љ–Њ—Б—В–Є) —Д–Є–Ї—Б–Є—А—Г—О—В 4% —Д–Њ—А–Љ–∞–ї–Є–љ–Њ–≤–Њ-—Б–њ–Є—А—В–Њ–≤—Л–Љ —А–∞—Б—В–≤–Њ—А–Њ–Љ –≤ —В–µ—З–µ–љ–Є–µ 30 —Б–µ–Ї—Г–љ–і.
* –Ю–±–Љ—Л–≤–∞—О—В –≤ –њ—А–Њ—В–Њ—З–љ–Њ–є –≤–Њ–і–µ –Є –≤—Л—Б—Г—И–Є–≤–∞—О—В.
* –Ч–∞–ї–Є–≤–∞—О—В –њ–µ—А–Њ–Ї—Б–Є–і–∞–Ј–љ—Л–Љ —А–µ–∞–Ї—В–Є–≤–Њ–Љ –љ–∞ 5 –Љ–Є–љ—Г—В.
* –Ґ—Й–∞—В–µ–ї—М–љ–Њ –њ—А–Њ–Љ—Л–≤–∞—О—В –≤ –њ—А–Њ—В–Њ—З–љ–Њ–є –≤–Њ–і–µ –Є –≤—Л—Б—Г—И–Є–≤–∞—О—В.
* –Ф–Њ–Ї—А–∞—И–Є–≤–∞—О—В –Ї—А–∞—Б–Є—В–µ–ї–µ–Љ –†–Њ–Љ–∞–љ–Њ–≤—Б–Ї–Њ–≥–Њ-–У–Є–Љ–Ј—Л.
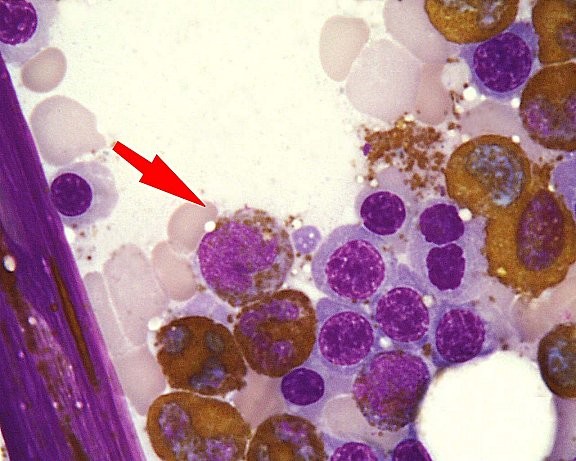
* –Ь–Є–µ–ї–Њ–њ–µ—А–Њ–Ї—Б–Є–і–∞–Ј–∞ –≤—Л—П–≤–ї—П–µ—В—Б—П –≤ —Ж–Є—В–Њ–њ–ї–∞–Ј–Љ–µ –Ї–ї–µ—В–Њ–Ї –≤ –≤–Є–і–µ –Ї–Њ—А–Є—З–љ–µ–≤—Л—Е –≥—А–∞–љ—Г–ї.
–Ь–Њ–і–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л–є –Љ–µ—В–Њ–і –Э–∞—А—Ж–Є—Б—Б–Њ–≤–∞ –†. –Я.
–Я—А–Є–љ—Ж–Є–њ:
–Т –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є –њ–µ—А–Њ–Ї—Б–Є–і–∞–Ј—Л –±–µ–љ–Ј–Є–і–Є–љ –Њ–Ї–Є—Б–ї—П–µ—В—Б—П –њ–µ—А–µ–Ї–Є—Б—М—О –≤–Њ–і–Њ—А–Њ–і–∞ –≤ –Ї–Њ—А–Є—З–љ–µ–≤—Л–є –Њ–Ї—Б–Є–±–µ–љ–Ј–Є–і–Є–љ. –Ф–ї—П —Г–Љ–µ–љ—М—И–µ–љ–Є—П –Є–љ–∞–Ї—В–Є–≤–∞—Ж–Є–Є —Д–µ—А–Љ–µ–љ—В–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ—Л —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є–є —Д–Є–Ї—Б–∞—В–Њ—А –Є –љ–µ–±–Њ–ї—М—И–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –њ–µ—А–µ–Ї–Є—Б–Є –≤–Њ–і–Њ—А–Њ–і–∞.
–†–µ–∞–Ї—В–Є–≤—Л
* 60% –≤–Њ–і–љ—Л–є —А–∞—Б—В–≤–Њ—А –∞—Ж–µ—В–Њ–љ–∞.
* 0,1 M —А–∞—Б—В–≤–Њ—А –±–Њ—А–∞—В–∞ –љ–∞—В—А–Є—П (–Љ–Њ–ґ–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М —Д–Њ—Б—Д–∞—В–љ—Л–є –Є–ї–Є –Љ–µ–і–Є–љ–∞–ї–Њ–≤—Л–є –±—Г—Д–µ—А–љ—Л–є —А–∞—Б—В–≤–Њ—А pH 7,6).
* –Ш–љ–Ї—Г–±–∞—Ж–Є–Њ–љ–љ–∞—П —Б—А–µ–і–∞: 5 –Љ–ї 5% –≤–Њ–і–љ–Њ–≥–Њ —А–∞—Б—В–≤–Њ—А–∞ —В—А–Є–ї–Њ–љ–∞ –С, 10 –Љ–ї —А–∞—Б—В–≤–Њ—А–∞ –±–Њ—А–∞—В–∞ –љ–∞—В—А–Є—П, 35 –Љ–ї –љ–∞—Б—Л—Й–µ–љ–љ–Њ–≥–Њ —А–∞—Б—В–≤–Њ—А–∞ –±–µ–љ–Ј–Є–і–Є–љ–∞ –Є 2 –Љ–ї 0,003% —А–∞—Б—В–≤–Њ—А–∞ –њ–µ—А–µ–Ї–Є—Б–Є –≤–Њ–і–Њ—А–Њ–і–∞ (–≥–Њ—В–Њ–≤—П—В –Є–Ј 3% —А–∞—Б—В–≤–Њ—А–∞ —А–∞–Ј–≤–µ–і–µ–љ–Є–µ–Љ –≤ –і–≤–∞ —Н—В–∞–њ–∞ –њ–µ—А–µ–і —Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є–µ–Љ).
* 0,5% —А–∞—Б—В–≤–Њ—А –Љ–µ—В–Є–ї–Њ–≤–Њ–≥–Њ –Ј–µ–ї–µ–љ–Њ–≥–Њ –љ–∞ –±—Г—Д–µ—А–љ–Њ–Љ —А–∞—Б—В–≤–Њ—А–µ (pH 5,0) –Є–ї–Є 0,1% –≤–Њ–і–љ—Л–є —А–∞—Б—В–≤–Њ—А –Љ–µ—В–Є–ї–µ–љ–Њ–≤–Њ–≥–Њ —Б–Є–љ–µ–≥–Њ.
–•–Њ–і –Њ–Ї—А–∞—Б–Ї–Є
* –°–≤–µ–ґ–µ–њ—А–Є–≥–Њ—В–Њ–≤–ї–µ–љ–љ—Л–µ –Љ–∞–Ј–Ї–Є —Д–Є–Ї—Б–Є—А—Г—О—В –≤ 60% –≤–Њ–і–љ–Њ–Љ —А–∞—Б—В–≤–Њ—А–µ –∞—Ж–µ—В–Њ–љ–∞ –≤ —В–µ—З–µ–љ–Є–µ 30 —Б–µ–Ї—Г–љ–і.
* –Я—А–Њ–Љ—Л–≤–∞—О—В –і–Є—Б—В–Є–ї–ї–Є—А–Њ–≤–∞–љ–љ–Њ–є –≤–Њ–і–Њ–є.
* –Ш–љ–Ї—Г–±–Є—А—Г—О—В –≤ –Є–љ–Ї—Г–±–∞—Ж–Є–Њ–љ–љ–Њ–є —Б—А–µ–і–µ –≤ —В–µ—З–µ–љ–Є–µ 1 —З–∞—Б–∞ –≤ —В–µ—А–Љ–Њ—Б—В–∞—В–µ –њ—А–Є 37 ¬∞C.
* –Я—А–Њ–Љ—Л–≤–∞—О—В –і–Є—Б—В–Є–ї–ї–Є—А–Њ–≤–∞–љ–љ–Њ–є –≤–Њ–і–Њ–є.
* –Ф–Њ–Ї—А–∞—И–Є–≤–∞—О—В –Љ–∞–Ј–Ї–Є –Љ–µ—В–Є–ї–Њ–≤—Л–Љ –Ј–µ–ї–µ–љ—Л–Љ –Є–ї–Є –Љ–µ—В–Є–ї–µ–љ–Њ–≤—Л–Љ —Б–Є–љ–Є–Љ –≤ —В–µ—З–µ–љ–Є–µ 10 –Љ–Є–љ—Г—В.
–Ь–Њ–і–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л–є –Љ–µ—В–Њ–і –®–∞—Д—А–∞–љ –Ь. –У. –Є —Б–Њ–∞–≤—В–Њ—А–Њ–≤
–Я—А–Є–љ—Ж–Є–њ:
–Њ–Ї–Є—Б–ї–µ–љ–Є–µ –Ю-–і–Є–∞–љ–Є–Ј–Є–і–Є–љ–∞ –њ–µ—А–µ–Ї–Є—Б—М—О –≤–Њ–і–Њ—А–Њ–і–∞ –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є –Љ–Є–µ–ї–Њ–њ–µ—А–Њ–Ї—Б–Є–і–∞–Ј—Л.
–†–µ–∞–Ї—В–Є–≤—Л
* 10% —Б–њ–Є—А—В–Њ–≤–Њ–є —А–∞—Б—В–≤–Њ—А —Д–Њ—А–Љ–∞–ї–Є–љ–∞ (1 –Љ–ї 10% —Д–Њ—А–Љ–∞–ї–Є–љ–∞ –Є 9 –Љ–ї —Н—В–Є–ї–Њ–≤–Њ–≥–Њ —Б–њ–Є—А—В–∞).
* –°–њ–Є—А—В–Њ–≤–Њ–є —А–∞—Б—В–≤–Њ—А –Ю-–і–Є–∞–љ–Є–Ј–Є–і–Є–љ–∞:
24 –Љ–≥ –Ю-–і–Є–∞–љ–Є–Ј–Є–і–Є–љ–∞ —А–∞—Б—В–≤–Њ—А—П—О—В –≤ 5 –Љ–ї –Љ–µ—В–∞–љ–Њ–ї–∞ –Є –і–Њ–≤–Њ–і—П—В –і–Є—Б—В–Є–ї–ї–Є—А–Њ–≤–∞–љ–љ–Њ–є –≤–Њ–і–Њ–є –і–Њ 9,9 –Љ–ї.
* 3% —А–∞—Б—В–≤–Њ—А –њ–µ—А–µ–Ї–Є—Б–Є –≤–Њ–і–Њ—А–Њ–і–∞.
* –†–µ–∞–Ї—Ж–Є–Њ–љ–љ–∞—П —Б–Љ–µ—Б—М: –Ї —Б–њ–Є—А—В–Њ–≤–Њ–Љ—Г —А–∞—Б—В–≤–Њ—А—Г –Ю-–і–Є–∞–љ–Є–Ј–Є–і–Є–љ–∞ –њ—А–Є–±–∞–≤–ї—П—О—В –њ–µ—А–µ–і —Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є–µ–Љ 0,1 –Љ–ї –њ–µ—А–µ–Ї–Є—Б–Є –≤–Њ–і–Њ—А–Њ–і–∞.
* 0,25% –≤–Њ–і–љ—Л–є —А–∞—Б—В–≤–Њ—А –∞–Ј—Г—А–∞ –Р –Є–ї–Є –і—А—Г–≥–Њ–є —П–і–µ—А–љ—Л–є –Ї—А–∞—Б–Є—В–µ–ї—М.
–•–Њ–і –Њ–Ї—А–∞—Б–Ї–Є
* –Ь–∞–Ј–Ї–Є —Д–Є–Ї—Б–Є—А—Г—О—В —Б–њ–Є—А—В–Њ–≤—Л–Љ —А–∞—Б—В–≤–Њ—А–Њ–Љ —Д–Њ—А–Љ–∞–ї–Є–љ–∞ –≤ —В–µ—З–µ–љ–Є–µ 10 - 15 —Б–µ–Ї—Г–љ–і.
* –°–њ–Њ–ї–∞—Б–Ї–Є–≤–∞—О—В –њ—А–Њ—В–Њ—З–љ–Њ–є –≤–Њ–і–Њ–є.
* –Э–∞ –Љ–∞–Ј–Ї–Є –љ–∞–љ–Њ—Б—П—В —А–µ–∞–Ї—Ж–Є–Њ–љ–љ—Г—О —Б–Љ–µ—Б—М –љ–∞ 2 вАФ 3 –Љ–Є–љ –њ—А–Є –Ї–Њ–Љ–љ–∞—В–љ–Њ–є —В–µ–Љ–њ–µ—А–∞—В—Г—А–µ.
* –°–њ–Њ–ї–∞—Б–Ї–Є–≤–∞—О—В –њ—А–Њ—В–Њ—З–љ–Њ–є –≤–Њ–і–Њ–є.
* –Ф–Њ–Ї—А–∞—И–Є–≤–∞—О—В —А–∞—Б—В–≤–Њ—А–Њ–Љ –∞–Ј—Г—А–∞ –≤ —В–µ—З–µ–љ–Є–µ 10 вАФ 15 —Б–µ–Ї—Г–љ–і.
* –°–њ–Њ–ї–∞—Б–Ї–Є–≤–∞—О—В –њ—А–Њ—В–Њ—З–љ–Њ–є –≤–Њ–і–Њ–є –Є –≤—Л—Б—Г—И–Є–≤–∞—О—В.
–Э–Њ—А–Љ–∞–ї—М–љ—Л–µ –≤–µ–ї–Є—З–Є–љ—Л –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Љ–Є–µ–ї–Њ–њ–µ—А–Њ–Ї—Б–Є–і–∞–Ј—Л
–Т –Ї—А–Њ–≤–Є –Ј–і–Њ—А–Њ–≤—Л—Е –ї—О–і–µ–є 3 вАФ 16% –љ–µ–є—В—А–Њ—Д–Є–ї–Њ–≤ –Є–Љ–µ—О—В —А–µ–Ј–Ї–Њ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Г—О, 60 вАФ 90% - —Г–Љ–µ—А–µ–љ–љ–Њ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Г—О, –Њ—Б—В–∞–ї—М–љ—Л–µ вАФ —Б–ї–∞–±–Њ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Г—О —А–µ–∞–Ї—Ж–Є—О –љ–∞ –Љ–Є–µ–ї–Њ–њ–µ—А–Њ–Ї—Б–Є–і–∞–Ј—Г. –°–¶–Ъ –љ–µ–є—В—А–Њ—Д–Є–ї–Њ–≤ –Ј–і–Њ—А–Њ–≤—Л—Е –ї—О–і–µ–є —А–∞–≤–µ–љ 2,23 вАФ 2,89. –£ –і–µ—В–µ–є –≤ –≤–Њ–Ј—А–∞—Б—В–µ 7 –ї–µ—В –°–¶–Ъ —Б–Њ—Б—В–∞–≤–ї—П–µ—В 2,03 вАФ 2,11, –Ї –њ–µ—А–Є–Њ–і—Г –њ–Њ–ї–Њ–≤–Њ–≥–Њ —Б–Њ–Ј—А–µ–≤–∞–љ–Є—П —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П —Г –Љ–∞–ї—М—З–Є–Ї–Њ–≤ –і–Њ 2,163 вАФ 2,237, –∞ —Г –і–µ–≤–Њ—З–µ–Ї —Г–Љ–µ–љ—М—И–∞–µ—В—Б—П –і–Њ 1,949 вАФ 2,011, –Ї 15 –≥–Њ–і–∞–Љ –њ–Њ–ї–Њ–≤—Л–µ —А–∞–Ј–ї–Є—З–Є—П –≤—Л—А–∞–≤–љ–Є–≤–∞—О—В—Б—П.
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Љ–Є–µ–ї–Њ–њ–µ—А–Њ–Ї—Б–Є–і–∞–Ј—Л
–†–µ–∞–Ї—Ж–Є—П –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –≥–ї–∞–≤–љ—Л–Љ –Њ–±—А–∞–Ј–Њ–Љ —Б —Ж–µ–ї—М—О –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Њ—Б—В—А—Л—Е –ї–µ–є–Ї–Њ–Ј–Њ–≤. –Я—А–Є –Њ—Б—В—А—Л—Е –Љ–Є–µ–ї–Њ–±–ї–∞—Б—В–љ—Л—Е –ї–µ–є–Ї–Њ–Ј–∞—Е –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Љ–Є–µ–ї–Њ–њ–µ—А–Њ–Ї—Б–Є–і–∞–Ј—Л –≤ –Њ–њ—Г—Е–Њ–ї–µ–≤—Л—Е –Ї–ї–µ—В–Ї–∞—Е –≤–∞—А—М–Є—А—Г–µ—В –Њ—В —Б–ї–∞–±–Њ–є –і–Њ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —Б—В–µ–њ–µ–љ–Є –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–Ї–Є –±–ї–∞—Б—В–Њ–≤. –Ґ–∞–Ї, –њ—А–Є –Њ—Б—В—А–Њ–Љ –Љ–Є–µ–ї–Њ–±–ї–∞—Б—В–љ–Њ–Љ –ї–µ–є–Ї–Њ–Ј–µ —Б –љ–Є–Ј–Ї–Њ–є —Б—В–µ–њ–µ–љ—М—О –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–Ї–Є –±–ї–∞—Б—В–Њ–≤ (M1 –њ–Њ –§–Р–С-–Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є–Є), –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –њ–µ—А–Њ–Ї—Б–Є–і–∞–Ј–Њ–њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л—Е –±–ї–∞—Б—В–Њ–≤ –љ–µ–≤–µ–ї–Є–Ї–Њ (–љ–µ –њ—А–µ–≤—Л—И–∞–µ—В 10%), —Б—В–µ–њ–µ–љ—М –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —Д–µ—А–Љ–µ–љ—В–∞ –≤ –љ–Є—Е –љ–µ–≤—Л—Б–Њ–Ї–∞—П. –Ґ–Њ–≥–і–∞ –Ї–∞–Ї –њ—А–Є –Њ—Б—В—А–Њ–Љ –њ—А–Њ–Љ–Є–µ–ї–Њ—Ж–Є—В–∞—А–љ–Њ–Љ –ї–µ–є–Ї–Њ–Ј–µ (M3 –њ–Њ –§–Р–С-–Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є–Є) –Љ–Є–µ–ї–Њ–њ–µ—А–Њ–Ї—Б–Є–і–∞–Ј–∞ –≤—Л—П–≤–ї—П–µ—В—Б—П –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –≤ 100% –±–ї–∞—Б—В–љ—Л—Е –Ї–ї–µ—В–Њ–Ї, –њ—А–Є—З–µ–Љ –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –µ–µ —А–∞–≤–љ–Њ–Ј–љ–∞—З–љ–∞ —В–∞–Ї–Њ–≤–Њ–є –≤ –Ј—А–µ–ї—Л—Е –љ–µ–є—В—А–Њ—Д–Є–ї–∞—Е. –Ю–і–љ–∞–Ї–Њ –Њ—В—Б—Г—В—Б—В–≤–Є–µ —В–Њ—З–љ—Л—Е –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ—Л—Е —Б–њ–Њ—Б–Њ–±–Њ–≤ –Њ—Ж–µ–љ–Ї–Є —Ж–Є—В–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е —А–µ–∞–Ї—Ж–Є–є –љ–µ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –Є—Е –і–ї—П –≤–µ—А–Є—Д–Є–Ї–∞—Ж–Є–Є —Б—В–µ–њ–µ–љ–Є –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–Ї–Є –±–ї–∞—Б—В–љ—Л—Е –Ї–ї–µ—В–Њ–Ї, –∞ —Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, –Є –±–Њ–ї–µ–µ —В–Њ–љ–Ї–Њ–є –і–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Њ—Б—В—А—Л—Е –ї–µ–є–Ї–Њ–Ј–Њ–≤. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Б –њ–Њ–Љ–Њ—Й—М—О —Ж–Є—В–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е —А–µ–∞–Ї—Ж–Є–є –Њ–њ—А–µ–і–µ–ї—П—О—В –ї–Є–љ–µ–є–љ—Г—О –љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ—Б—В—М, –∞ –љ–µ —Б—В–µ–њ–µ–љ—М –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–Ї–Є –±–ї–∞—Б—В–Њ–≤.
–Я—А–Є –Њ—Б—В—А—Л—Е –Љ–Њ–љ–Њ–±–ї–∞—Б—В–љ—Л—Е –ї–µ–є–Ї–Њ–Ј–∞—Е —А–µ–∞–Ї—Ж–Є—П –љ–∞ –Љ–Є–µ–ї–Њ–њ–µ—А–Њ–Ї—Б–Є–і–∞–Ј—Г –≤ –Њ–њ—Г—Е–Њ–ї–µ–≤—Л—Е –Ї–ї–µ—В–Ї–∞—Е —Б–ї–∞–±–∞—П, –њ—А–Є –Њ—Б—В—А—Л—Е –ї–Є–Љ—Д–Њ–±–ї–∞—Б—В–љ—Л—Е –ї–µ–є–Ї–Њ–Ј–∞—Е вАФ –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ–∞—П.
–°–љ–Є–ґ–µ–љ–Є–µ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —Д–µ—А–Љ–µ–љ—В–∞ –≤ –љ–µ–є—В—А–Њ—Д–Є–ї–∞—Е –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ –њ—А–Є –Є–љ—Д–∞—А–Ї—В–µ –Љ–Є–Њ–Ї–∞—А–і–∞, —А–µ–≤–Љ–∞—В–Є–Ј–Љ–µ, —В—Г–±–µ—А–Ї—Г–ї–µ–Ј–µ, –Њ–њ—Г—Е–Њ–ї—П—Е. –£ –±–Њ–ї—М–љ—Л—Е —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ –Љ–Є–µ–ї–Њ–ї–µ–є–Ї–Њ–Ј–Њ–Љ, –Њ—Б–Њ–±–µ–љ–љ–Њ –≤ —В–µ—А–Љ–Є–љ–∞–ї—М–љ–Њ–є —Б—В–∞–і–Є–Є, –°–¶–Ъ —Б–љ–Є–ґ–∞–µ—В—Б—П –і–Њ 1,44 вАФ 1,82.

|