–Э–µ–є—А–Њ–≥–Є—Б—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Љ–µ—В–Њ–і—Л –≤ –Є–Ј—Г—З–µ–љ–Є–µ –Љ–Њ–Ј–≥–∞ –Є –њ–Њ–≤–µ–і–µ–љ–Є—П
–У–Ш–°–Ґ–Ю–Ы–Ю–У–Ш–І–Х–°–Ъ–Ш–Х –Ш –Э–Х–Щ–†–Ю–Р–Э–Р–Ґ–Ю–Ь–Ш–І–Х–°–Ъ–Ш–Х –Ь–Х–Ґ–Ю–Ф–Ђ
–Т–Њ –Љ–љ–Њ–≥–Є—Е –Њ–њ—Л—В–∞—Е –Є –Љ–µ—В–Њ–і–∞—Е, –њ–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—О –Љ–Њ–Ј–≥–∞ –Є –њ–Њ–≤–µ–і–µ–љ–Є—П, –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ—В—Б—П –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ–µ –Љ–∞–љ–Є–њ—Г–ї–Є—А–Њ–≤–∞–љ–Є–µ —Б –Љ–Њ–Ј–≥–Њ–Љ, –Ї–∞–Ї, –љ–∞–њ—А–Є–Љ–µ—А, –≤–≤–µ–і–µ–љ–Є–µ —Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–Є—Е –Є–ї–Є —А–µ–≥–Є—Б—В—А–Є—А—Г—О—Й–Є—Е —Н–ї–µ–Ї—В—А–Њ–і–Њ–≤, –Є–љ—К–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е –Ї–∞–љ—О–ї—М –Є –љ–∞–љ–µ—Б–µ–љ–Є–µ —А–∞–Ј–ї–Є—З–љ—Л—Е —В–Є–њ–Њ–≤ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–є. –Т –і–∞–љ–љ–Њ–є –≥–ї–∞–≤–µ –њ—А–Є–≤–µ–і–µ–љ—Л –Њ—Б–љ–Њ–≤–љ—Л–µ –≥–Є—Б—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Љ–µ—В–Њ–і–Є–Ї–Є, –Ї–Њ—В–Њ—А—Л–µ –њ—А–Є–Љ–µ–љ—П—О—В—Б—П –і–ї—П —Г—В–Њ—З–љ–µ–љ–Є—П –њ–Њ–ї–Њ–ґ–µ–љ–Є—П –Є–Љ–њ–ї–∞–љ—В–Є—А–Њ–≤–∞–љ–љ—Л—Е —Н–ї–µ–Ї—В—А–Њ–і–Њ–≤ –Є –Ї–∞–љ—О–ї—М –Є –і–ї—П –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П –Њ–±—К–µ–Љ–∞ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е —А–∞–Ј—А—Г—И–µ–љ–Є–є –Љ–Њ–Ј–≥–∞
–Я–Х–†–§–£–Ч–Ш–ѓ
–Ю–±–Њ—А—Г–і–Њ–≤–∞–љ–Є–µ.
–•–Є–Љ–Є—З–µ—Б–Ї–Є–µ –љ–Њ–ґ–љ–Є—Ж—Л (–±–Њ–ї—М—И–Є–µ –Є –Љ–∞–ї—Л–µ), –і–≤–µ –њ–ї–∞—Б—В–Љ–∞—Б—Б–Њ–≤—Л–µ –±—Г—В—Л–ї–Ї–Є (2вАФ5 –ї), —А–µ–Ј–Є–љ–Њ–≤–∞—П —В—А—Г–±–Ї–∞ –Є —В—А–µ—Е–Ї–∞–љ–∞–ї—М–љ—Л–є –≤–µ–љ—В–Є–ї—М.
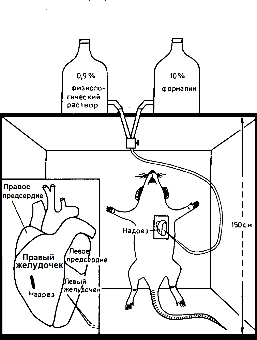
–†–Є—Б. 1. –°–Є—Б—В–µ–Љ–∞ –і–ї—П –њ–µ—А—Д—Г–Ј–Є–Є
–Я–µ—А—Д—Г–Ј–Є—А–Њ–≤–∞–љ–Є–µ –ґ–Є–≤–Њ—В–љ–Њ–≥–Њ –њ—А–Њ–Є–Ј–≤–Њ–і–Є—В—Б—П —З–µ—А–µ–Ј —Б–Є—Б—В–µ–Љ—Г –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П –і–ї—П –і–Њ—Б—В–∞–≤–Ї–Є –≤—Л–±—А–∞–љ–љ–Њ–≥–Њ —Д–Є–Ї—Б–∞—В–Њ—А–∞ (–љ–∞–њ—А–Є–Љ–µ—А, –≥–ї—Г—В–∞—А–Њ–≤—Л–є –∞–ї—М–і–µ–≥–Є–і, —Н—В–∞–љ–Њ–ї –Є —Д–Њ—А–Љ–∞–ї–Є–љ). –Ц–Є–і–Ї–Њ—Б—В—М –њ–Њ—Б—В—Г–њ–∞–µ—В –њ–Њ–і –і–∞–≤–ї–µ–љ–Є–µ–Љ, –Ї–Њ—В–Њ—А–Њ–µ –њ—А–Є–Љ–µ—А–љ–Њ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г–µ—В –љ–Њ—А–Љ–∞–ї—М–љ–Њ–Љ—Г –Ї—А–Њ–≤—П–љ–Њ–Љ—Г –і–∞–≤–ї–µ–љ–Є—О –ґ–Є–≤–Њ—В–љ–Њ–≥–Њ. –≠—В–Њ –і–Њ—Б—В–Є–≥–∞–µ—В—Б—П, –µ—Б–ї–Є, –љ–∞–њ—А–Є–Љ–µ—А, –њ–Њ–і–≤–µ—Б–Є—В—М –±—Г—В—Л–ї—М, —Б–Њ–і–µ—А–ґ–∞—Й—Г—О –њ–µ—А—Д—Г–Ј–Є—А—Г—О—Й—Г—О –ґ–Є–і–Ї–Њ—Б—В—М, –љ–∞ –≤—Л—Б–Њ—В—Г –Њ–Ї–Њ–ї–Њ 150 —Б–Љ –љ–∞–і –ґ–Є–≤–Њ—В–љ—Л–Љ. –Я–µ—А—Д—Г–Ј–Є–Њ–љ–љ–∞—П —Б–Є—Б—В–µ–Љ–∞ –њ–Њ–Ї–∞–Ј–∞–љ–∞ –љ–∞ —А–Є—Б. 1.2; –Њ–љ–∞ —Б–Њ—Б—В–Њ–Є—В –Є–Ј –і–≤—Г—Е –±—Г—В—Л–ї–µ–є (–Њ–і–љ–∞ —Б–Њ–і–µ—А–ґ–Є—В —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є —А–∞—Б—В–≤–Њ—А, –∞ –і—А—Г–≥–∞—П вАФ –њ–µ—А—Д—Г–Ј–Є—А—Г—О—Й—Г—О –ґ–Є–і–Ї–Њ—Б—В—М), —А–∞–Ј–і–≤–∞–Є–≤–∞—О—Й–µ–є—Б—П —Б–Є—Б—В–µ–Љ—Л —А–µ–Ј–Є–љ–Њ–≤—Л—Е –Є–ї–Є –њ–Њ–ї–Є—Н—В–Є–ї–µ–љ–Њ–≤—Л—Е —В—А—Г–±–Њ–Ї –Є —В—А–µ—Е–Ї–∞–љ–∞–ї—М–љ–Њ–≥–Њ –≤–µ–љ—В–Є–ї—П.
–Ґ—А–µ—Е–Ї–∞–љ–∞–ї—М–љ—Л–є –≤–µ–љ—В–Є–ї—М –њ–Њ–Ј–≤–Њ–ї—П–µ—В –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ –≤–ї–Є–≤–∞—В—М —А–∞–Ј–ї–Є—З–љ—Л–µ —А–∞—Б—В–≤–Њ—А—Л. –Т –њ–µ—А—Д—Г–Ј–Є–Њ–љ–љ–Њ–є —Б–Є—Б—В–µ–Љ–µ –≤–∞–ґ–љ–Њ –љ–µ –і–Њ–њ—Г—Б–Ї–∞—В—М –њ–Њ—П–≤–ї–µ–љ–Є—П –њ—Г–Ј—Л—А—М–Ї–Њ–≤ –≤–Њ–Ј–і—Г—Е–∞.
–Я–µ—А–µ–і –њ–µ—А—Д—Г–Ј–Є—А–Њ–≤–∞–љ–Є–µ–Љ –љ–∞—А–Ї–Њ—В–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–µ –ґ–Є–≤–Њ—В–љ–Њ–µ –Ї–ї–∞–і–µ—В—Б—П –љ–∞ —Б–њ–Є–љ—Г, –љ–∞ –µ–≥–Њ –≥—А—Г–і–љ–Њ–є –Ї–ї–µ—В–Ї–µ –і–µ–ї–∞–µ—В—Б—П –љ–∞–і—А–µ–Ј (—Б–њ—А–∞–≤–∞ –Є —Б–ї–µ–≤–∞ –Њ—В –≥—А—Г–і–Є–љ—Л). –Ъ–∞–љ—О–ї—П, –њ—А–Є–Ї—А–µ–њ–ї–µ–љ–љ–∞—П –Ї —А–µ–Ј–Є–љ–Њ–≤–Њ–є —В—А—Г–±–Ї–µ, –≤–≤–Њ–і–Є—В—Б—П –Ј–∞—В–µ–Љ –≤ –ї–µ–≤—Л–є –ґ–µ–ї—Г–і–Њ—З–µ–Ї, –Є –љ–∞—З–Є–љ–∞–µ—В—Б—П –њ–Њ–і–∞—З–∞ —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —А–∞—Б—В–≤–Њ—А–∞. –Т –њ—А–∞–≤–Њ–Љ –ґ–µ–ї—Г–і–Њ—З–Ї–µ –і–ї—П –і–∞–ї—М–љ–µ–є—И–µ–≥–Њ –±—Л—Б—В—А–Њ–≥–Њ –Ј–∞–Љ–µ—Й–µ–љ–Є—П –Ї—А–Њ–≤–Є —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ —А–∞—Б—В–≤–Њ—А–Њ–Љ (—А–Є—Б. 1) –і–µ–ї–∞—О—В –љ–µ–±–Њ–ї—М—И–Њ–є –љ–∞–і—А–µ–Ј.
–Я–Њ—Б–ї–µ —В–Њ–≥–Њ –Ї–∞–Ї —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є —А–∞—Б—В–≤–Њ—А –≤—Л–Љ—Л–ї –Ї—А–Њ–≤—М, —Д–Њ—А–Љ–∞–ї–Є–љ–Њ–≤–∞—П –њ–µ—А—Д—Г–Ј–Є—А—Г—О—Й–∞—П –ґ–Є–і–Ї–Њ—Б—В—М –љ–∞—З–Є–љ–∞–µ—В –њ–Њ—Б—В—Г–њ–∞—В—М —З–µ—А–µ–Ј —Б–Є—Б—В–µ–Љ—Г –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П –ґ–Є–≤–Њ—В–љ–Њ–≥–Њ.
–Ю —В–Њ–Љ, —З—В–Њ –њ–µ—А—Д—Г–Ј–Є—А–Њ–≤–∞–љ–Є–µ –њ—А–Њ–≤–µ–і–µ–љ–Њ –њ—А–∞–≤–Є–ї—М–љ–Њ, –Љ–Њ–ґ–љ–Њ —Г–Ј–љ–∞—В—М –њ–Њ —А–µ–∞–Ї—Ж–Є–Є –њ–µ—А—Д—Г–Ј–Є—А—Г—О—Й–µ–є –ґ–Є–і–Ї–Њ—Б—В–Є —Б –±–µ–ї–Ї–∞–Љ–Є –Ї–ї–µ—В–Њ–Ї, –≤—Л–Ј—Л–≤–∞—О—Й–µ–є —В—А–µ–Љ–Њ—А –Љ—Л—И—Ж. –Ъ–Њ–≥–і–∞ –ґ–Є–≤–Њ—В–љ–Њ–µ –Њ–Ї–Њ—Б—В–µ–љ–µ–≤–∞–µ—В –Є –Њ–±—К–µ–Љ –њ—А–Њ–њ—Г—Й–µ–љ–љ–Њ–є –њ–µ—А—Д—Г–Ј–Є—А—Г—О—Й–µ–є –ґ–Є–і–Ї–Њ—Б—В–Є —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г–µ—В –µ–≥–Њ —Г—В—А–Њ–±–љ–Њ–є –Љ–∞—Б—Б–µ, –Љ–Њ–ґ–љ–Њ —Г–і–∞–ї—П—В—М –Љ–Њ–Ј–≥ –Є–Ј —З–µ—А–µ–њ–∞.
–Ф–ї—П –њ—А–Є–≥–Њ—В–Њ–≤–ї–µ–љ–Є—П 10%-–љ–Њ–≥–Њ –Ј–∞–±—Г—Д–µ—А–µ–љ–љ–Њ–≥–Њ —А–∞—Б—В–≤–Њ—А–∞ —Д–Њ—А–Љ–∞–ї—М–і–µ–≥–Є–і–∞ (pH 7,3вАФ7,5) –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —А–∞—Б—В–≤–Њ—А–Є—В—М 9 –≥ NaCl, 4 –≥ –Љ–Њ–љ–Њ–≥–Є–і—А–∞—В–∞ –і–Є–≥–Є–і—А–Њ—Д–Њ—Б—Д–∞—В–∞ –љ–∞—В—А–Є—П (NaH2P04-H20) –Є 8,35 –≥ –і–Є–≥–Є–і—А–∞—В–∞ –≥–Є–і—А–Њ—Д–Њ—Б—Д–∞—В–∞ –љ–∞—В—А–Є—П (Na2HP04-H20) –≤ 900 –Љ–ї –і–Є—Б—В–Є–ї–ї–Є—А–Њ–≤–∞–љ–љ–Њ–є –≤–Њ–і—Л; –Ј–∞—В–µ–Љ –і–Њ–±–∞–≤–Є—В—М 100 –Љ–ї –≥–Њ—В–Њ–≤–Њ–≥–Њ —А–∞—Б—В–≤–Њ—А–∞ —Д–Њ—А–Љ–∞–ї–Є–љ–∞ (37,5%). –Ґ–∞–Ї–Њ–є 10%-–љ—Л–є —А–∞—Б—В–≤–Њ—А –Ј–∞–±—Г—Д–µ—А–µ–љ–љ–Њ–≥–Њ —Д–Њ—А–Љ–∞–ї—М–і–µ–≥–Є–і–∞ –њ—А–Є–≥–Њ—В–∞–≤–ї–Є–≤–∞–µ—В—Б—П –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є —В–Њ–≥–Њ, —З—В–Њ –Њ–±—Л—З–љ—Л–є –≥–Њ—В–Њ–≤—Л–є —Д–Њ—А–Љ–∞–ї—М–і–µ–≥–Є–і –Є–Љ–µ–µ—В 37,5%-–љ—Г—О –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—О. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П 10%-–љ–Њ–≥–Њ —Д–Њ—А–Љ–∞–ї–Є–љ–∞ —Б–Њ—Б—В–∞–≤–ї—П–µ—В 3,75% –Ј–∞–±—Г—Д–µ—А–µ–љ–љ–Њ–≥–Њ —А–∞—Б—В–≤–Њ—А–∞ —Д–Њ—А–Љ–∞–ї—М–і–µ–≥–Є–і–∞. –†–∞—Б—В–≤–Њ—А —Е—А–∞–љ–Є—В—Б—П –≤ –њ—А–Њ—Е–ї–∞–і–љ–Њ–Љ –Љ–µ—Б—В–µ.
–Я—А–Є –±–Њ–ї—М—И–µ–Љ pH —Г–Љ–µ–љ—М—И–∞–µ—В—Б—П –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ —Б–≤—П–Ј–∞–љ–љ–Њ–≥–Њ –±–µ–ї–Ї–∞ –≤ –Ї–ї–µ—В–Ї–∞—Е –Є —В–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ —Б–љ–Є–ґ–∞–µ—В—Б—П –Ї–∞—З–µ—Б—В–≤–Њ –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–≥–Њ –Њ–Ї—А–∞—И–Є–≤–∞–љ–Є—П, —В–∞–Ї –Ї–∞–Ї –±–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –њ—А–Њ—Ж–µ–і—Г—А –Њ–Ї—А–∞—И–Є–≤–∞–љ–Є—П –Ј–∞–≤–Є—Б–Є—В –Њ—В —А–µ–∞–Ї—Ж–Є–Є —Б –±–µ–ї–Ї–∞–Љ–Є. –Я–Њ—Н—В–Њ–Љ—Г —Д–Њ—А–Љ–∞–ї–Є–љ –і–µ–є—Б—В–≤—Г–µ—В –љ–∞–Є–±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ –≤ –≤–Є–і–µ –Ј–∞–±—Г—Д–µ—А–µ–љ–љ–Њ–≥–Њ 10%-–љ–Њ–≥–Њ —А–∞—Б—В–≤–Њ—А–∞, pH –Ї–Њ—В–Њ—А–Њ–≥–Њ 7,5.
–Х—Б–ї–Є –њ–µ—А—Д—Г–Ј–Є—П –љ–µ —Г–і–∞–ї–∞—Б—М, –≥–Њ–ї–Њ–≤—Г –ґ–Є–≤–Њ—В–љ–Њ–≥–Њ –Њ—В–і–µ–ї—П—О—В –Њ—В —В—Г–ї–Њ–≤–Є—Й–∞ –Є —А–∞—Б–Ї—А—Л–≤–∞—О—В —З–µ—А–µ–њ –Ї–∞–Ї –Љ–Њ–ґ–љ–Њ –њ–Њ–ї–љ–µ–µ. –Ч–∞—В–µ–Љ –≥–Њ–ї–Њ–≤—Г –њ–Њ–Љ–µ—Й–∞—О—В –≤ 10%-–љ—Л–є –Ј–∞–±—Г—Д–µ—А–µ–љ–љ—Л–є —А–∞—Б—В–≤–Њ—А —Д–Њ—А–Љ–∞–ї–Є–љ–∞ –Є –Љ–Њ–Ј–≥ –Ј–∞—В–≤–µ—А–і–µ–≤–∞–µ—В, –љ–∞—Е–Њ–і—П—Б—М –њ—А–Є —Н—В–Њ–Љ –≤ —З–µ—А–µ–њ–µ.
–Я—А–Њ—Ж–µ–і—Г—А–∞ –Ј–∞–љ–Є–Љ–∞–µ—В 1вАФ2 –љ–µ–і–µ–ї–Є. –Я–Њ—Б–ї–µ —Н—В–Њ–≥–Њ –Љ–Њ–Ј–≥ –Њ—Б—В–Њ—А–Њ–ґ–љ–Њ –Є–Ј–≤–ї–µ–Ї–∞—О—В (—Б–Љ. —А–∞–Ј–і–µ–ї 1.4.2) –Є–Ј —З–µ—А–µ–њ–∞ –Є —Г–і–∞–ї—П—О—В —В–≤–µ—А–і—Г—О –Љ–Њ–Ј–≥–Њ–≤—Г—О –Њ–±–Њ–ї–Њ—З–Ї—Г. –Ь–Њ–Ј–≥ —А–µ–ґ—Г—В –љ–∞ –±–ї–Њ–Ї–Є —В–Њ–ї—Й–Є–љ–Њ–є –Њ–Ї–Њ–ї–Њ 5 –Љ–Љ; –±–ї–Њ–Ї–Є –Њ—Б—В–∞–≤–ї—П—О—В –≤ 10%-–љ–Њ–Љ –Ј–∞–±—Г—Д–µ—А–µ–љ–љ–Њ–Љ —Д–Њ—А–Љ–∞–ї–Є–љ–µ –µ—Й–µ –љ–∞ –і–≤–µ –љ–µ–і–µ–ї–Є. –Ф–∞–ї–µ–µ —Б–ї–µ–і—Г–µ—В –і–µ–є—Б—В–≤–Њ–≤–∞—В—М —В–∞–Ї –ґ–µ, –Ї–∞–Ї –≤ —Б–ї—Г—З–∞–µ –Є–љ—В—А–∞–Ї–∞—А–і–Є–∞–ї—М–љ–Њ–є –њ–µ—А—Д—Г–Ј–Є–Є –ґ–Є–≤–Њ—В–љ–Њ–≥–Њ.
–Ш–Ч–Т–Ы–Х–І–Х–Э–Ш–Х –Ь–Ю–Ч–У–Р
–Ш–љ—Б—В—А—Г–Љ–µ–љ—В—Л. –С–Њ–ї—М—И–Є–µ —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є–µ –љ–Њ–ґ–љ–Є—Ж—Л, –њ–Є–љ—Ж–µ—В –Є —Г–Ј–Ї–Є–µ –Ї—Г—Б–∞—З–Ї–Є.
–Ю—В—Б–µ–Ї–Є—В–µ –≥–Њ–ї–Њ–≤—Г –ґ–Є–≤–Њ—В–љ–Њ–≥–Њ –Є —Г–і–∞–ї–Є—В–µ —Б—В–Њ–ї—М–Ї–Њ –Љ—Л—И—Ж, —Б–Ї–Њ–ї—М–Ї–Њ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –і–ї—П –Њ–±–љ–∞–ґ–µ–љ–Є—П —З–µ—А–µ–њ–∞. –Я–Њ–і—Ж–µ–њ–Є—В–µ –Є–Љ–њ–ї–∞–љ—В–Є—А–Њ–≤–∞–љ–љ—Л–µ —Н–ї–µ–Ї—В—А–Њ–і—Л –Є–ї–Є –Ї–∞–љ—О–ї–Є –њ–µ–∞–љ–Њ–Љ –Є –Њ—Б—В–Њ—А–Њ–ґ–љ–Њ —Б–љ–Є–Љ–Є—В–µ –Є—Е —Б —З–µ—А–µ–њ–∞ –≤–Љ–µ—Б—В–µ —Б –Ј–∞–Ї—А–µ–њ–ї—П—О—Й–Є–Љ –Ј—Г–±–љ—Л–Љ —Ж–µ–Љ–µ–љ—В–Њ–Љ. –Э–∞—З–Є–љ–∞–є—В–µ —Г–і–∞–ї—П—В—М –Ї–Њ—Б—В—М, –ї–µ–ґ–∞—Й—Г—О –љ–∞–і —Б—В–≤–Њ–ї–Њ–Љ –Љ–Њ–Ј–≥–∞, –Њ—Б—В–Њ—А–Њ–ґ–љ–Њ –Њ—В—Ж–µ–њ–ї—П—П –µ–µ –Ї—Г—Б–∞—З–Ї–∞–Љ–Є. –£–і–∞–ї–Є—В–µ —Б—В–Њ–ї—М–Ї–Њ –Ї–Њ—Б—В–Є, —Б–Ї–Њ–ї—М–Ї–Њ –љ—Г–ґ–љ–Њ, —З—В–Њ–±—Л –Љ–Њ–ґ–љ–Њ –±—Л–ї–Њ –њ—А–Є–њ–Њ–і–љ—П—В—М –Љ–Њ–Ј–≥ –Є –њ–µ—А–µ—А–µ–Ј–∞—В—М —З–µ—А–µ–њ–љ—Л–µ –љ–µ—А–≤—Л –љ–Њ–ґ–љ–Є—Ж–∞–Љ–Є. –Я–Њ–Љ–µ—Б—В–Є—В–µ –Љ–Њ–Ј–≥ –≤ 10%-–љ—Л–є —А–∞—Б—В–≤–Њ—А —Д–Њ—А–Љ–∞–ї–Є–љ–∞ –љ–∞ –Њ–і–Є–љ –і–µ–љ—М, –њ—А–µ–ґ–і–µ —З–µ–Љ –љ–∞—З–љ–µ—В–µ —А–∞–±–Њ—В–∞—В—М —Б –љ–Є–Љ. –Я–µ—А–µ–і —В–µ–Љ –Ї–∞–Ї —А–∞–Ј—А–µ–Ј–∞—В—М –Љ–Њ–Ј–≥, –њ–Њ–Љ–µ—В—М—В–µ –Њ–і–љ–Њ –њ–Њ–ї—Г—И–∞—А–Є–µ –њ—А–Њ–і–Њ–ї—М–љ—Л–Љ —А–∞–Ј—А–µ–Ј–Њ–Љ —Б–±–Њ–Ї—Г, —З—В–Њ–±—Л –љ–µ –њ–µ—А–µ–њ—Г—В–∞—В—М –њ–Њ–ї—Г—И–∞—А–Є—П.
–Ш–Ч–У–Ю–Ґ–Ю–Т–Ы–Х–Э–Ш–Х –С–Ы–Ю–Ъ–Ю–Т –Ґ–Ъ–Р–Э–Ш –Ь–Ю–Ч–У–Р
–Я—А–Њ—Б–ї–µ–ґ–Є–≤–∞–љ–Є–µ —Н–ї–µ–Ї—В—А–Њ–і–љ—Л—Е —В—А–µ–Ї–Њ–≤ –Є –Є–і–µ–љ—В–Є—Д–Є–Ї–∞—Ж–Є—П —А–∞–Ј—А—Г—И–µ–љ–љ—Л—Е —Г—З–∞—Б—В–Ї–Њ–≤ –Љ–Њ–Ј–≥–∞ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –Њ–±–ї–µ–≥—З–∞–µ—В—Б—П, –µ—Б–ї–Є –і–µ–ї–∞—В—М —Б—А–µ–Ј—Л –њ–∞—А–∞–ї–ї–µ–ї—М–љ–Њ –њ–ї–Њ—Б–Ї–Њ—Б—В–Є –њ–Њ–≥—А—Г–ґ–µ–љ–Є—П —Н–ї–µ–Ї—В—А–Њ–і–Њ–≤ –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б–Њ —Б—В–µ—А–µ–Њ—В–∞–Ї—Б–Є—З–µ—Б–Ї–Є–Љ –∞—В–ї–∞—Б–Њ–Љ, –Ї–Њ—В–Њ—А—Л–є
–Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї—Б—П –≤–Њ –≤—А–µ–Љ—П –Њ–њ—Л—В–∞. –Ф–ї—П —Н—В–Њ–≥–Њ –Љ–Њ–Ј–≥ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —А–∞–Ј—А–µ–Ј–∞—В—М –љ–∞ –љ–µ–Ї–Њ—В–Њ—А–Њ–Љ —А–∞—Б—Б—В–Њ—П–љ–Є–Є –Њ—В —Г—З–∞—Б—В–Ї–∞, –њ—А–µ–і—Б—В–∞–≤–ї—П—О—Й–µ–≥–Њ –Є–љ—В–µ—А–µ—Б, –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–µ–є –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–є –њ–ї–Њ—Б–Ї–Њ—Б—В–Є.
–†–Є—Б.3. –£—Б—В—А–Њ–є—Б—В–≤–Њ –і–ї—П –Є–Ј–≥–Њ—В–Њ–≤–ї–µ–љ–Є—П –±–ї–Њ–Ї–Њ–≤ —В–Ї–∞–љ–Є
 
|
–° –њ–Њ–Љ–Њ—Й—М—О –і–≤—Г—Е —В–∞–Ї–Є—Е —А–∞–Ј—А–µ–Ј–Њ–≤, —Б–і–µ–ї–∞–љ–љ—Л—Е –љ–∞ —А–∞—Б—Б—В–Њ—П–љ–Є–Є 2вАФ3 –Љ–Љ –Ї–њ–µ—А–µ–і–Є –Є –Ї–Ј–∞–і–Є –Њ—В —В–Њ–є —З–∞—Б—В–Є –Љ–Њ–Ј–≥–∞, –Ї–Њ—В–Њ—А–∞—П –Є—Б—Б–ї–µ–і—Г–µ—В—Б—П –≥–Є—Б—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є, –Њ—В–і–µ–ї—П—О—В –±–ї–Њ–Ї —В–Ї–∞–љ–Є, –Ї–Њ—В–Њ—А—Л–є –Љ–Њ–ґ–љ–Њ —Б—А–∞–Ј—Г –њ–µ—А–µ–љ–µ—Б—В–Є –љ–∞ —Б—В–Њ–ї–Є–Ї –Ј–∞–Љ–Њ—А–∞–ґ–Є–≤–∞—О—Й–µ–≥–Њ –Љ–Є–Ї—А–Њ—В–Њ–Љ–∞. –Ґ–Њ—З–љ–Њ—Б—В—М —А–∞–Ј—А–µ–Ј–Њ–≤ –њ—А–Є –Є–Ј–≥–Њ—В–Њ–≤–ї–µ–љ–Є–Є –±–ї–Њ–Ї–Њ–≤ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –Є—Е –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–µ —Б—Е–Њ–і—Б—В–≤–Њ —Б –Ї–∞—А—В–∞–Љ–Є —Б—В–µ—А–µ–Њ—В–∞–Ї—Б–Є—З–µ—Б–Ї–Њ–≥–Њ –∞—В–ї–∞—Б–∞ –Є –њ–Њ–Ј–≤–Њ–ї—П–µ—В –њ—А–Њ—Б–ї–µ–і–Є—В—М –≤–µ—А—В–Є–Ї–∞–ї—М–љ—Л–µ —В—А–µ–Ї–Є –љ–∞ –Њ—В–і–µ–ї—М–љ–Њ–Љ —Б—А–µ–Ј–µ –њ–Њ –≤—Б–µ–є –Є—Е –і–ї–Є–љ–µ.
–Ф–ї—П –≤–Њ—Б–њ—А–Њ–Є–Ј–≤–µ–і–µ–љ–Є—П —Б—В–µ—А–µ–Њ—В–∞–Ї—Б–Є—З–µ—Б–Ї–Є—Е –Ї–Њ–Њ—А–і–Є–љ–∞—В, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є—Е —А–∞–Ј–Љ–µ—А–∞–Љ —З–µ—А–µ–њ–∞, –Є–Ј–≤–ї–µ—З–µ–љ–љ—Л–є –Љ–Њ–Ј–≥ –≤ –њ–µ—А–µ–≤–µ—А–љ—Г—В–Њ–Љ –≤–Є–і–µ –њ–Њ–Љ–µ—Й–∞—О—В –љ–∞ –≥–Њ—А–Є–Ј–Њ–љ—В–∞–ї—М–љ—Г—О –њ–ї–∞—Б—В–Є–љ–Ї—Г. –Я–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –Љ–Њ–Ј–ґ–µ—З–Ї–∞ –Є –±–Њ–ї—М—И–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—В –њ–ї–Њ—Б–Ї–Њ—Б—В–Є –±—А–µ–≥–Љ–∞-–ї—П–Љ–±–і–∞, –∞ –њ–Њ–≥—А–∞–љ–Є—З–љ–∞—П –ї–Є–љ–Є—П –Љ–µ–ґ–і—Г –Љ–Њ–Ј–ґ–µ—З–Ї–Њ–Љ –Є –±–Њ–ї—М—И–Є–Љ –Љ–Њ–Ј–≥–Њ–Љ —Г–Ї–∞–Ј—Л–≤–∞–µ—В –љ–∞ —Г—А–Њ–≤–µ–љ—М –ї—П–Љ–±–і—Л. –Э–∞ —А–Є—Б.3 –њ—А–Є–≤–µ–і–µ–љ–Њ –њ—А–Њ—Б—В–Њ–µ –њ—А–Є—Б–њ–Њ—Б–Њ–±–ї–µ–љ–Є–µ, —Г–і–Њ–±–љ–Њ–µ –і–ї—П —А–∞–Ј—А–µ–Ј–∞–љ–Є—П –Љ–Њ–Ј–≥–∞ –Ї—А—Л—Б—Л –љ–∞ –±–ї–Њ–Ї–Є. –Ю–љ–Њ —Б–Њ—Б—В–Њ–Є—В –Є–Ј —Г–Ј–Ї–Њ–є –Ї–∞–Љ–µ—А—Л, –Є–Ј–≥–Њ—В–Њ–≤–ї–µ–љ–љ–Њ–є –Є–Ј –њ–ї–µ–Ї—Б–Є–≥–ї–∞—Б–∞ (20X30X25) [–Љ–Љ], —Б –≤–µ—А—В–Є–Ї–∞–ї—М–љ—Л–Љ–Є –њ—А–Њ—А–µ–Ј—П–Љ–Є (S) —И–Є—А–Є–љ–Њ–є 0,3 –Љ–Љ, —Б–і–µ–ї–∞–љ–љ—Л–Љ–Є –≤ –±–Њ–Ї–Њ–≤—Л—Е —Б—В–µ–љ–Ї–∞—Е —Б —А–µ–≥—Г–ї—П—А–љ—Л–Љ –Є–љ—В–µ—А–≤–∞–ї–Њ–Љ –≤ 1 –Љ–Љ. –Я–ї–µ–Ї—Б–Є–≥–ї–∞—Б–Њ–≤–∞—П –њ–ї–∞—В—Д–Њ—А–Љ–∞ (–†) –Љ–Њ–ґ–µ—В –±—Л—В—М –љ–∞–Ї–ї–Њ–љ–µ–љ–∞ —В–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —З—В–Њ –≤–µ—А—Е–љ–Є–µ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –Љ–Њ–Ј–ґ–µ—З–Ї–∞ –Є –њ–Њ–ї—Г—И–∞—А–Є–є –±–Њ–ї—М—И–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ —А–∞—Б–њ–Њ–ї–∞–≥–∞—О—В—Б—П –њ–Њ –Њ—В–љ–Њ—И–µ–љ–Є—О –Ї –≤–µ—А—В–Є–Ї–∞–ї—М–љ—Л–Љ –њ—А–Њ—А–µ–Ј—П–Љ –њ–Њ–і —Г–≥–ї–Њ–Љ —Б—А, —З—В–Њ —В–∞–Ї–ґ–µ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–µ –Є—Б–њ–Њ–ї—М–Ј—Г–µ–Љ–Њ–Љ—Г —Б—В–µ—А–µ–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–Љ—Г –∞—В–ї–∞—Б—Г. –Ы–µ–Ј–≤–Є–µ–Љ –±—А–Є—В–≤—Л, –≤—Б—В–∞–≤–ї–µ–љ–љ–Њ–є –≤ –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–µ –Њ—В–≤–µ—А—Б—В–Є—П –≤ —Б—В–µ–љ–Ї–∞—Е –Ї–∞–Љ–µ—А—Л, —А–∞–Ј—А–µ–Ј–∞—О—В –Љ–Њ–Ј–≥ –≤ –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–є –њ–ї–Њ—Б–Ї–Њ—Б—В–Є –љ–∞ –љ—Г–ґ–љ–Њ–Љ —Г—А–Њ–≤–љ–µ.
–Ш–Ч–У–Ю–Ґ–Ю–Т–Ы–Х–Э–Ш–Х –°–†–Х–Ч–Ю–Т
–Ь–µ—В–Њ–і –Є–Ј–≥–Њ—В–Њ–≤–ї–µ–љ–Є—П –Ј–∞–Љ–Њ—А–Њ–ґ–µ–љ–љ—Л—Е —Б—А–µ–Ј–Њ–≤ —И–Є—А–Њ–Ї–Њ –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –Є –Њ—В–≤–µ—З–∞–µ—В –Љ–љ–Њ–≥–Є–Љ —Ж–µ–ї—П–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П. –Я–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Љ–µ—В–Њ–і–∞–Љ–Є –Ј–∞–ї–Є–≤–Ї–Є –Љ–Њ–Ј–≥–∞ –≤ –њ–∞—А–∞—Д–Є–љ –Є —Ж–µ–ї–ї–Њ–Є–і–Є–љ –µ–≥–Њ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ–Љ —П–≤–ї—П–µ—В—Б—П —В–Њ, —З—В–Њ –њ–Њ–і–≥–Њ—В–Њ–≤–Ї–∞ –Ї –Є–Ј–≥–Њ—В–Њ–≤–ї–µ–љ–Є—О —Б—А–µ–Ј–Њ–≤ –Ј–∞–љ–Є–Љ–∞–µ—В –Љ–∞–ї–Њ –≤—А–µ–Љ–µ–љ–Є, —Б –њ–Њ–Љ–Њ—Й—М—О –Љ–µ—В–Њ–і–∞ –Ј–∞–Љ–Њ—А–Њ–ґ–µ–љ–љ—Л—Е —Б—А–µ–Ј–Њ–≤ —В–Ї–∞–љ—М –Њ–±—Л—З–љ–Њ —А–µ–ґ—Г—В —В–Њ–ї—Й–Є–љ–Њ–є –Њ—В 25 –і–Њ 100 –Љ–Ї–Љ. –Х—Б–ї–Є —Б—А–µ–Ј—Л –і–Њ–ї–ґ–љ—Л –±—Л—В—М –±–Њ–ї–µ–µ —В–Њ–љ–Ї–Є–Љ–Є, —В–Њ –Љ–Њ–Ј–≥ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Ј–∞–ї–Є–≤–∞—В—М –≤ –њ–∞—А–∞—Д–Є–љ, —З—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Є–Ј–≥–Њ—В–Њ–≤–ї—П—В—М —Б—А–µ–Ј—Л —В–Њ–ї—Й–Є–љ–Њ–є –Њ—В 2 –і–Њ 15 –Љ–Ї–Љ.
1. –Ю–±–µ–Ј–≤–Њ–ґ–Є–≤–∞–љ–Є–µ –Љ–Њ–Ј–≥–∞ –Є –Ј–∞–ї–Є–≤–Ї–∞ –µ–≥–Њ –≤ –њ–∞—А–∞—Д–Є–љ
–Ф–ї—П –Є–Ј–≥–Њ—В–Њ–≤–ї–µ–љ–Є—П —Б—А–µ–Ј–Њ–≤ –Є–Ј –љ–µ–Ј–∞–Љ–Њ—А–Њ–ґ–µ–љ–љ–Њ–≥–Њ –Љ–∞—В–µ—А–Є–∞–ї–∞ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–∞ –≥–Њ–Љ–Њ–≥–µ–љ–љ–∞—П —Б—В–∞–±–Є–ї—М–љ–Њ—Б—В—М –Љ–Њ–Ј–≥–Њ–≤—Л—Е —Б—В—А—Г–Ї—В—Г—А. –Ґ–Њ–љ–Ї–Є–µ –Є —А–∞–≤–љ–Њ–Љ–µ—А–љ—Л–µ —Б—А–µ–Ј—Л –Љ–Њ–≥—Г—В –±—Л—В—М –њ–Њ–ї—Г—З–µ–љ—Л –њ—Г—В–µ–Љ –Ј–∞–ї–Є–≤–Ї–Є –Љ–Њ–Ј–≥–∞ –≤ –њ–∞—А–∞—Д–Є–љ (–њ–∞—А–∞–њ–ї–∞—Б—В) (—Б–Љ. —В–∞–Ї–ґ–µ Humason, 1979).
–Ґ–∞–Ї –Ї–∞–Ї –Љ–Њ–Ј–≥ —Б–Њ–і–µ—А–ґ–Є—В –Њ—В 70 (–≤ –≤–Њ–ї–Њ–Ї–љ–∞—Е) –і–Њ 80% –≤–Њ–і—Л (–≤ –Ї–ї–µ—В–Ї–∞—Е), —В–Њ –µ–≥–Њ –љ—Г–ґ–љ–Њ –Њ–±–µ–Ј–≤–Њ–ґ–Є–≤–∞—В—М, –Ј–∞–Љ–µ—Й–∞—П –≤–Њ–і—Г –Ј–∞–ї–Є–≤–Њ—З–љ—Л–Љ –Љ–∞—В–µ—А–Є–∞–ї–Њ–Љ. –Ф–ї—П —Г–і–∞–ї–µ–љ–Є—П –≤–Њ–і—Л –Љ–Њ–ґ–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М —Б–Њ–µ–і–Є–љ–µ–љ–Є—П, –Њ–±–ї–∞–і–∞—О—Й–Є–µ –±–Њ–ї—М—И–Є–Љ —Б—А–Њ–і—Б—В–≤–Њ–Љ –Ї –љ–µ–є (–љ–∞–њ—А–Є–Љ–µ—А, —Н—В–∞–љ–Њ–ї). –І—В–Њ–±—Л —Б–≤–µ—Б—В–Є –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–µ —В–Ї–∞–љ–Є –і–Њ –Љ–Є–љ–Є–Љ—Г–Љ–∞, —Н—В–Є —Б–Њ–µ–і–Є–љ–µ–љ–Є—П –Є—Б–њ–Њ–ї—М–Ј—Г—О—В –≤ –≤–Њ–Ј—А–∞—Б—В–∞—О—Й–Є—Е –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П—Е. –Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ –њ—А–Є –Њ–±—А–∞–±–Њ—В–Ї–µ –Љ–Њ–Ј–≥ —Г–Љ–µ–љ—М—И–∞–µ—В—Б—П –≤ –Њ–±—К–µ–Љ–µ –њ–Њ—З—В–Є –љ–∞ 7%. –Т –Ї–∞—З–µ—Б—В–≤–µ –њ—А–Є–Љ–µ—А–∞ –Њ–±–µ–Ј–≤–Њ–ґ–Є–≤–∞–љ–Є—П –Є–Ј–Њ–њ—А–Њ–њ–∞–љ–Њ–ї–Њ–Љ (–Є–Ј–Њ–њ—А–Њ–њ–Є–ї–Њ–≤—Л–є —Б–њ–Є—А—В) –Є –Ј–∞–ї–Є–≤–Ї–Є –≤ –њ–∞—А–∞–њ–ї–∞—Б—В (–њ–∞—А–∞—Д–Є–љ) –њ—А–Є–≤–Њ–і–Є—В—Б—П —Б–ї–µ–і—Г—О—Й–∞—П –њ—А–Њ—Ж–µ–і—Г—А–∞:
–Ф–µ–љ—М
| –Т—А–µ–Љ—П, —З
| –Ю–±—А–∞–±–Њ—В–Ї–∞
|
| 11,00
| –Ш–Ј–Њ–њ—А–Њ–њ–∞–љ–Њ–ї (50%-–љ—Л–є)
| 1
| 21,00
| –Ш–Ј–Њ–њ—А–Њ–њ–∞–љ–Њ–ї (75%-–љ—Л–є)
| 2
| 11,00
| –Ш–Ј–Њ–њ—А–Њ–њ–∞–љ–Њ–ї (96%-–љ—Л–є)
| 3
| 11,00
| –Ш–Ј–Њ–њ—А–Њ–њ–∞–љ–Њ–ї (96%-–љ—Л–є)
| 4
| 11,00
| –Ш–Ј–Њ–њ—А–Њ–њ–∞–љ–Њ–ї (100%-–љ—Л–є)
| 5
| 11,00
| –Ь–µ—В–Є–ї–±–µ–љ–Ј–Њ–∞—В
|
| 19,00
| –С–µ–љ–Ј–Њ–ї
|
| 19,30
| –С–µ–љ–Ј–Њ–ї –њ–∞—А–∞–њ–ї–∞—Б—В
|
| 21,00
| –Я–∞—А–∞–њ–ї–∞—Б—В (—А–∞—Б–њ–ї–∞–≤–ї–µ–љ–љ—Л–є –њ–∞—А–∞—Д–Є–љ) 56вАФ58¬∞–°
| 6
| 19,00
| –Я—А–Є–≥–Њ—В–Њ–≤–ї–µ–љ–Є–µ –±–ї–Њ–Ї–Њ–≤ –≤ –Ї–Њ—А–Њ–±–Ї–µ –Є–Ј –∞–ї—О–Љ–Є–љ–Є–µ–≤–Њ–є —Д–Њ–ї—М–≥–Є
|
–Я–Њ—Б–ї–µ —В–Њ–≥–Њ –Ї–∞–Ї –±–ї–Њ–Ї –Ј–∞—В–≤–µ—А–і–µ–µ—В, –Ј–∞–ї–Є—В—Л–є –Љ–Њ–Ј–≥ –≥–Њ—В–Њ–≤ –і–ї—П –Є–Ј–≥–Њ—В–Њ–≤–ї–µ–љ–Є—П —Б—А–µ–Ј–Њ–≤.
2. –Ш–Ј–≥–Њ—В–Њ–≤–ї–µ–љ–Є–µ –Ј–∞–Љ–Њ—А–Њ–ґ–µ–љ–љ—Л—Е —Б—А–µ–Ј–Њ–≤
–Ф–ї—П –Є–Ј–≥–Њ—В–Њ–≤–ї–µ–љ–Є—П –Ј–∞–Љ–Њ—А–Њ–ґ–µ–љ–љ—Л—Е —Б—А–µ–Ј–Њ–≤ (–≤ –Ї—А–Є–Њ—Б—В–∞—В–µ –Є–ї–Є –љ–∞ –Ј–∞–Љ–Њ—А–∞–ґ–Є–≤–∞—О—Й–µ–Љ –Љ–Є–Ї—А–Њ—В–Њ–Љ–µ) –Љ–Њ–Ј–≥ –Њ–±—А–∞–±–∞—В—Л–≤–∞–µ—В—Б—П —А–∞—Б—В–≤–Њ—А–∞–Љ–Є —Д–Њ—А–Љ–∞–ї–Є–љ–∞ —Б —Б–∞—Е–∞—А–Њ–Ј–Њ–є –≤ —Б–ї–µ–і—Г—О—Й–µ–Љ –њ–Њ—А—П–і–Ї–µ.
–Я–Њ—Б–ї–µ –Є–Ј–≤–ї–µ—З–µ–љ–Є—П –Є–Ј —З–µ—А–µ–њ–∞ –Љ–Њ–Ј–≥ —Б–љ–∞—З–∞–ї–∞ –њ–Њ–Љ–µ—Й–∞—О—В –≤ 100%- –љ—Л–є —А–∞—Б—В–≤–Њ—А —Б–∞—Е–∞—А–Њ–Ј—Л —Б —Д–Њ—А–Љ–∞–ї–Є–љ–Њ–Љ (–°–§) (100 –≥ —Б–∞—Е–∞—А–Њ–Ј—Л –љ–∞ 1000 –Љ–ї 10%-–љ–Њ–≥–Њ –Ј–∞–±—Г—Д–µ—А–µ–љ–љ–Њ–≥–Њ —А–∞—Б—В–≤–Њ—А–∞ —Д–Њ—А–Љ–∞–ї–Є–љ–∞). –Э–∞ —Б–ї–µ–і—Г—О—Й–Є–є –і–µ–љ—М –Љ–Њ–Ј–≥ –њ–µ—А–µ–љ–Њ—Б—П—В –≤ 20%-–љ—Л–є —А–∞—Б—В–≤–Њ—А –°–§, –∞ –љ–∞ —В—А–µ—В–Є–євАФ –≤ 30%-–љ—Л–є. –Ю–±—К–µ–Љ —А–∞—Б—В–≤–Њ—А–∞ –°–§ –і–Њ–ї–ґ–µ–љ –њ—А–Є–Љ–µ—А–љ–Њ –≤ 20 —А–∞–Ј –њ—А–µ–≤—Л—И–∞—В—М –Њ–±—К–µ–Љ –Љ–Њ–Ј–≥–∞. –Ь–Њ–Ј–≥ –Љ–Њ–ґ–љ–Њ –њ–µ—А—Д—Г–Ј–Є—А–Њ–≤–∞—В—М —В–∞–Ї–ґ–µ 5%- –љ—Л–Љ —А–∞—Б—В–≤–Њ—А–Њ–Љ —Д–Њ—А–Љ–∞–ї–Є–љ–∞, –∞ –Ј–∞—В–µ–Љ –њ–Њ–Љ–µ—Б—В–Є—В—М –µ–≥–Њ –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ –≤ 30%-–љ—Л–є –°–§. –°–∞—Е–∞—А–Њ–Ј–∞ –Љ–µ—И–∞–µ—В –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—О –Ї—А–Є—Б—В–∞–ї–ї–Њ–≤ –ї—М–і–∞ –њ—А–Є –Є–Ј–≥–Њ—В–Њ–≤–ї–µ–љ–Є–Є —Б—А–µ–Ј–Њ–≤. –≠—В–Є –Ї—А–Є—Б—В–∞–ї–ї—Л —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Г—Е—Г–і—И–∞—О—В –Ї–∞—З–µ—Б—В–≤–Њ —Б—А–µ–Ј–Њ–≤. –Ъ–∞–Ї —В–Њ–ї—М–Ї–Њ –Љ–Њ–Ј–≥ –њ—А–Њ–њ–Є—В–∞–µ—В—Б—П 30%-–љ—Л–Љ –°–§, –µ–≥–Њ —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–∞—П –Љ–∞—Б—Б–∞ –љ–∞—З–Є–љ–∞–µ—В –њ—А–µ–≤—Л—И–∞—В—М –Љ–∞—Б—Б—Г —А–∞—Б—В–≤–Њ—А–∞ –Є –Њ–љ –њ–Њ–≥—А—Г–ґ–∞–µ—В—Б—П –љ–∞ –і–љ–Њ —Б–Њ—Б—Г–і–∞. –≠—В–Њ –Ј–љ–∞—З–Є—В, —З—В–Њ –Љ–Њ–Ј–≥ –≥–Њ—В–Њ–≤ –і–ї—П –Є–Ј–≥–Њ—В–Њ–≤–ї–µ–љ–Є—П —Б—А–µ–Ј–Њ–≤. –Ь–Њ–Ј–≥ –Љ–Њ–ґ–µ—В –Њ—Б—В–∞–≤–∞—В—М—Б—П –≤ —А–∞—Б—В–≤–Њ—А–µ –°–§ –≤ —В–µ—З–µ–љ–Є–µ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –љ–µ–і–µ–ї—М. –Х—Б–ї–Є –µ–≥–Њ —Е—А–∞–љ–Є—В—М —В–∞–Љ —Б–ї–Є—И–Ї–Њ–Љ –і–Њ–ї–≥–Њ, –Њ–љ —Б—В–∞–љ–Њ–≤–Є—В—Б—П —В–≤–µ—А–і—Л–Љ –Є –µ–≥–Њ —В—А—Г–і–љ–µ–µ —А–µ–Ј–∞—В—М.
–Э–µ–Ї–Њ—В–Њ—А—Г—О —Б–ї–Њ–ґ–љ–Њ—Б—В—М –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В –њ—А–Є–Ї—А–µ–њ–ї–µ–љ–Є–µ –Љ–Њ–Ј–≥–∞ –Ї –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є —Б—В–Њ–ї–Є–Ї–∞ –Љ–Є–Ї—А–Њ—В–Њ–Љ–∞. –Ю–і–Є–љ –Є–Ј —Б–њ–Њ—Б–Њ–±–Њ–≤ –љ–∞–і–µ–ґ–љ–Њ–є —Д–Є–Ї—Б–∞—Ж–Є–Є —В–Ї–∞–љ–Є –Љ–Њ–Ј–≥–∞ вАФ —Н—В–Њ –Є–Ј–≥–Њ—В–Њ–≤–ї–µ–љ–Є–µ –ґ–µ–ї–∞—В–Є–љ–Њ–≤–Њ–є –њ–Њ–і–ї–Њ–ґ–Ї–Є.
–Э–µ–Њ–±—Е–Њ–і–Є–Љ—Л —Б–ї–µ–і—Г—О—Й–Є–µ –Љ–∞—В–µ—А–Є–∞–ї—Л: 9 –љ–µ–±–Њ–ї—М—И–Є—Е –ї–Њ–ґ–µ–Ї –ґ–µ–ї–∞—В–Є–љ–∞ –Є 500 –Љ–ї –Э20. –°–Љ–µ—И–∞–є—В–µ –ґ–µ–ї–∞—В–Є–љ–Њ–≤—Л–є –њ–Њ—А–Њ—И–Њ–Ї —Б –≤–Њ–і–Њ–є, –њ—А–Њ–Ї–Є–њ—П—В–Є—В–µ –Є –≤—Л–ї–µ–є—В–µ –ґ–Є–і–Ї–Њ—Б—В—М –≤ –њ–ї–Њ—Б–Ї—Г—О —З–∞—И–µ—З–Ї—Г –і–ї—П –Љ–µ–і–ї–µ–љ–љ–Њ–≥–Њ –Ј–∞—Б—В—Л–≤–∞–љ–Є—П –њ—А–Є –Ї–Њ–Љ–љ–∞—В–љ–Њ–є —В–µ–Љ–њ–µ—А–∞—В—Г—А–µ. –Ц–µ–ї–∞—В–Є–љ –Љ–Њ–ґ–љ–Њ —Е—А–∞–љ–Є—В—М –≤ —Е–Њ–ї–Њ–і–Є–ї—М–љ–Є–Ї–µ, –њ—А–Є —Н—В–Њ–Љ –і–Њ–±–∞–≤–ї–µ–љ–Є–µ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –Ї–∞–њ–µ–ї—М —Д–Њ—А–Љ–∞–ї–Є–љ–∞ –њ—А–µ–њ—П—В—Б—В–≤—Г–µ—В –Ј–∞–њ–ї–µ—Б–љ–µ–≤–µ–љ–Є—О, –∞ –∞–ї—О–Љ–Є–љ–Є–µ–≤–∞—П —Д–Њ–ї—М–≥–∞ вАФ –≤—Л—Б—Л—Е–∞–љ–Є—О –ґ–µ–ї–∞—В–Є–љ–∞. –Х—Б–ї–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ, –ґ–µ–ї–∞—В–Є–љ –Љ–Њ–ґ–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –њ–Њ —З–∞—Б—В—П–Љ.
–°–ї–µ–≥–Ї–∞ –њ–Њ–і–Њ–≥—А–µ–є—В–µ –ґ–µ–ї–∞—В–Є–љ–Њ–≤—Г—О –њ–Њ–і–ї–Њ–ґ–Ї—Г –њ–Њ–і —Б—В—А—Г–µ–є –≤–Њ–і—Л –Є –њ–Њ–Љ–µ—Б—В–Є—В–µ –µ–µ –љ–∞ –Љ–Є–Ї—А–Њ—В–Њ–Љ–љ—Л–є —Б—В–Њ–ї–Є–Ї, –Љ–Њ–Ј–≥ –њ–Њ–ї–Њ–ґ–Є—В–µ —Б–≤–µ—А—Е—Г. –Ч–∞–Љ–Њ—А–∞–ґ–Є–≤–∞–љ–Є–µ –њ—А–Њ–Є–Ј–≤–Њ–і–Є—В–µ –Љ–µ–і–ї–µ–љ–љ–Њ –Є —А–∞–≤–љ–Њ–Љ–µ—А–љ–Њ, –ґ–µ–ї–∞—В–µ–ї—М–љ–Њ –љ–∞ –Љ–Є–Ї—А–Њ—В–Њ–Љ–µ, –Ј–∞–Љ–Њ—А–∞–ґ–Є–≤–∞—О—Й–µ–Љ —Б–љ–Є–Ј—Г. –Ъ–Њ–≥–і–∞ –Љ–Њ–Ј–≥ —Б—В–∞–љ–µ—В —В–≤–µ—А–і—Л–Љ –Є –Ј–∞–Љ–Њ—А–Њ–ґ–µ–љ–љ—Л–Љ, –µ–≥–Њ –Љ–Њ–ґ–љ–Њ —А–µ–Ј–∞—В—М. –Ґ–µ–Љ–њ–µ—А–∞—В—Г—А–∞ —А–µ–Ј–∞–љ–Є—П –і–Њ–ї–ґ–љ–∞ –±—Л—В—М –Њ—В вАФ7 –і–ЊвАФ15¬∞–°. –Х—Б–ї–Є —В–µ–Љ–њ–µ—А–∞—В—Г—А–∞ —Б–ї–Є—И–Ї–Њ–Љ –љ–Є–Ј–Ї–∞—П, —В–Њ —Б—А–µ–Ј—Л –ї–Є–±–Њ —Б–Ї—А—Г—З–Є–≤–∞—О—В—Б—П, –ї–Є–±–Њ –і–∞—О—В —В—А–µ—Й–Є–љ—Л.
–Ч–∞–Љ–Њ—А–Њ–ґ–µ–љ–љ—Л–µ —Б—А–µ–Ј—Л –Љ–Њ–≥—Г—В —В–∞–Ї–ґ–µ –Є–Ј–≥–Њ—В–Њ–≤–ї—П—В—М—Б—П –Є–Ј –±–ї–Њ–Ї–Њ–≤, –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е –њ—Г—В–µ–Љ –Ј–∞–ї–Є–≤–Ї–Є –Ї—Г—Б–Њ—З–Ї–∞ –Љ–Њ–Ј–≥–∞ –≤ –ґ–µ–ї–∞—В–Є–љ. –Ф–ї—П —Н—В–Њ–≥–Њ –Љ–Њ–Ј–≥ –Њ—Б—В–∞–≤–ї—П—О—В –≤ –≤–Њ–і–љ—Л—Е —А–∞—Б—В–≤–Њ—А–∞—Е –ґ–µ–ї–∞—В–Є–љ–∞ —Б –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П–Љ–Є 12,5 –Є 25% –≤ –Ї–∞–ґ–і–Њ–Љ —А–∞—Б—В–≤–Њ—А–µ –≤ —В–µ—З–µ–љ–Є–µ 6 —З –њ—А–Є +37¬∞–°. –Я–Њ—Б–ї–µ —Н—В–Њ–≥–Њ –Љ–Њ–Ј–≥ –њ–Њ–Љ–µ—Й–∞—О—В –≤ –љ–µ–±–Њ–ї—М—И—Г—О –±–∞–љ–Ї—Г, —Б–Њ–і–µ—А–ґ–∞—Й—Г—О 25%- –љ—Л–є –≤–Њ–і–љ—Л–є —А–∞—Б—В–≤–Њ—А –ґ–µ–ї–∞—В–Є–љ–∞, –Є —Е—А–∞–љ—П—В –≤ —Е–Њ–ї–Њ–і–Є–ї—М–љ–Є–Ї–µ. –Ч–∞–Ї—А–µ–њ–ї–µ–љ–љ—Л–є –≤ –ґ–µ–ї–∞—В–Є–љ–µ –Њ–±—А–∞–Ј–µ—Ж –Ј–∞—В–µ–Љ —А–µ–ґ–µ—В—Б—П –≤ –Ї—А–Є–Њ—Б—В–∞—В–µ.
–Т–∞–ґ–љ–Њ, —З—В–Њ–±—Л —В–Ї–∞–љ—М –љ–µ —А–∞–Ј—А—Л–≤–∞–ї–∞—Б—М, —Г–≥–Њ–ї –љ–∞–Ї–ї–Њ–љ–∞ –љ–Њ–ґ–∞ –њ—А–Є —А–µ–Ј–∞–љ–Є–Є –±—Л–ї –Њ–Ї–Њ–ї–Њ 30¬∞ . –Х—Б–ї–Є —Г–≥–Њ–ї –љ–∞–Ї–ї–Њ–љ–∞ —Б–ї–Є—И–Ї–Њ–Љ –≤–µ–ї–Є–Ї –Є–ї–Є —Б–ї–Є—И–Ї–Њ–Љ –Љ–∞–ї, —В–Њ —Б—А–µ–Ј –Љ–Њ–ґ–µ—В —Б–Љ–Њ—А—Й–Є—В—М—Б—П –Є–ї–Є –±—Л—В—М –љ–µ—А–Њ–≤–љ—Л–Љ. –†–µ–ґ—М—В–µ –Љ–µ–і–ї–µ–љ–љ–Њ –Є —Б–њ–Њ–Ї–Њ–є–љ–Њ. –Т—А–µ–Љ—П –Њ—В –≤—А–µ–Љ–µ–љ–Є –њ—А–Њ–і–Њ–ї–ґ–∞–є—В–µ –Ј–∞–Љ–Њ—А–Њ–Ј–Ї—Г –њ—А–Є –Є–Ј–≥–Њ—В–Њ–≤–ї–µ–љ–Є–Є —Б—А–µ–Ј–Њ–≤ —В–Њ–ї—Й–Є–љ–Њ–є 30 –Љ–Ї–Љ. –°—А–µ–Ј—Л —В–Ї–∞–љ–Є –Љ–Њ–Ј–≥–∞ –і–Њ–ї–ґ–љ—Л —Б–љ–Є–Љ–∞—В—М—Б—П —Б –љ–Њ–ґ–∞ –і–≤–Є–ґ–µ–љ–Є–µ–Љ –Ї–Є—Б—В–Њ—З–Ї–Є, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ—Л–Љ –Ї–љ–Є–Ј—Г. –°—В–∞—А–∞–є—В–µ—Б—М –љ–µ –њ—А–Є–Ї–∞—Б–∞—В—М—Б—П –Ї–Є—Б—В–Њ—З–Ї–Њ–є –Ї –ї–µ–Ј–≤–Є—О –љ–Њ–ґ–∞, —В–∞–Ї –Ї–∞–Ї –Љ–Њ–ґ–љ–Њ –њ–Њ–≤—А–µ–і–Є—В—М –љ–Њ–ґ. –Я–Њ–Љ–µ—Б—В–Є—В–µ —Б—А–µ–Ј—Л —В–Ї–∞–љ–Є –≤ 0,5вАФ1,0%-–љ—Л–є —А–∞—Б—В–≤–Њ—А —Д–Њ—А–Љ–∞–ї–Є–љ–∞. –Э–∞ —Н—В–Њ–є —Б—В–∞–і–Є–Є —В–Ї–∞–љ—М –Љ–Њ–ґ–љ–Њ —Е—А–∞–љ–Є—В—М –≤ —Е–Њ–ї–Њ–і–Є–ї—М–љ–Є–Ї–µ –і–ї—П –і–∞–ї—М–љ–µ–є—И–µ–є –Њ–±—А–∞–±–Њ—В–Ї–Є —Б—А–µ–Ј–Њ–≤.
–Я–Ю–Ф–У–Ю–Ґ–Ю–Т–Ъ–Р –Ц–Х–Ы–Р–Ґ–Ш–Э–Ш–Ч–Ш–†–Ю–Т–Р–Э–Э–Ђ–• –Я–†–Х–Ф–Ь–Х–Ґ–Э–Ђ–• –°–Ґ–Х–Ъ–Ю–Ы
–Э–∞–Ї–ї–µ–Є–≤–∞–љ–Є–µ —Б—А–µ–Ј–Њ–≤ –Љ–Њ–Ј–≥–∞ –љ–∞ –њ—А–µ–і–Љ–µ—В–љ—Л–µ —Б—В–µ–Ї–ї–∞ –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–ї–Њ–ґ–љ—Г—О –њ—А–Њ—Ж–µ–і—Г—А—Г, –Ї–Њ—В–Њ—А–∞—П –Љ–Њ–ґ–µ—В –±—Л—В—М —А–µ—И–µ–љ–∞ –њ—Г—В–µ–Љ –ґ–µ–ї–∞—В–Є–љ–Є–Ј–Є—А–Њ–≤–∞–љ–Є—П —Н—В–Є—Е —Б—В–µ–Ї–Њ–ї. –≠—В–Њ —В—А—Г–і–Њ–µ–Љ–Ї–Є–є, –љ–Њ –љ–∞–і–µ–ґ–љ—Л–є –Љ–µ—В–Њ–і.
–Ь–∞—В–µ—А–Є–∞–ї—Л, –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л–µ –і–ї—П –Њ—З–Є—Б—В–Ї–Є –њ—А–µ–і–Љ–µ—В–љ—Л—Е —Б—В–µ–Ї–Њ–ї. 100 –≥ –і–Є—Е—А–Њ–Љ–∞—В–∞ –Ї–∞–ї–Є—П (–Ъ2Cr2–Ю7), 850 –Љ–ї –Э20 –Є 100 –Љ–ї —Б–µ—А–љ–Њ–є –Ї–Є—Б–ї–Њ—В—Л (H2SO4). –Ф–ї—П –њ—А–Є–≥–Њ—В–Њ–≤–ї–µ–љ–Є—П —А–∞—Б—В–≤–Њ—А–∞ —Е—А–Њ–Љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л —А–∞—Б—В–≤–Њ—А–Є—В–µ –і–Є—Е—А–Њ–Љ–∞—В –Ї–∞–ї–Є—П –≤ –≤–Њ–і–µ, –Ј–∞—В–µ–Љ –і–Њ–±–∞–≤—М—В–µ —Б–µ—А–љ—Г—О –Ї–Є—Б–ї–Њ—В—Г.
–Ь–∞—В–µ—А–Є–∞–ї—Л, –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л–µ –і–ї—П –њ–Њ–Ї—А—Л—В–Є—П –ґ–µ–ї–∞—В–Є–љ–Њ–Љ –њ—А–µ–і–Љ–µ—В–љ—Л—Е —Б—В–µ–Ї–Њ–ї. 10 –≥ –ґ–µ–ї–∞—В–Є–љ–∞ –≤ –њ–Њ—А–Њ—И–Ї–µ, 0,25 –≥ —Е—А–Њ–Љ–Њ–≤—Л—Е –Ї–≤–∞—Б—Ж–Њ–≤ –Є 500 –Љ–ї –і–Є—Б—В–Є–ї–ї–Є—А–Њ–≤–∞–љ–љ–Њ–є –≤–Њ–і—Л.
–Я—А–µ–і–Љ–µ—В–љ—Л–µ —Б—В–µ–Ї–ї–∞ –њ–Њ–Љ–µ—Й–∞—О—В –≤ —А–∞—Б—В–≤–Њ—А —Е—А–Њ–Љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –љ–∞ 48 —З. –Ц–µ–ї–∞—В–µ–ї—М–љ–Њ —Б—В–µ–Ї–ї–∞ —Б—В–∞–≤–Є—В—М –≤ —И—В–∞—В–Є–≤—Л —В–∞–Ї, —З—В–Њ–±—Л –Њ–љ–Є –љ–µ –Ї–∞—Б–∞–ї–Є—Б—М –і—А—Г–≥ –і—А—Г–≥–∞. –°—В–µ–Ї–ї–∞ –њ—А–Њ–Љ—Л–≤–∞—О—В –њ–Њ–і —Б—В—А—Г–µ–є –≥–Њ—А—П—З–µ–є –≤–Њ–і—Л –≤ —В–µ—З–µ–љ–Є–µ 2 —З, –∞ –Ј–∞–≥–µ–Љ –≤ —В–µ—З–µ–љ–Є–µ 15 –Љ–Є–љвАФ–і–µ–Є–Њ–љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–є –≤–Њ–і–Њ–є. –Я—А–µ–і–Љ–µ—В–љ—Л–µ —Б—В–µ–Ї–ї–∞ –і–Њ–ї–ґ–љ—Л –њ–Њ–ї–љ–Њ—Б—В—М—О –≤—Л—Б–Њ—Е–љ—Г—В—М, –љ–Њ —В–∞–Ї, —З—В–Њ–±—Л –љ–∞ –љ–Є—Е –љ–µ –њ–Њ–њ–∞–ї–∞ –њ—Л–ї—М. –Ф–∞–ї–µ–µ –Є—Е –і–≤–∞–ґ–і—Л –њ–Њ–≥—А—Г–ґ–∞—О—В –≤ —В–µ–њ–ї—Л–є –ґ–µ–ї–∞—В–Є–љ (—Б–њ–Њ—Б–Њ–± –µ–≥–Њ –њ—А–Є–≥–Њ—В–Њ–≤–ї–µ–љ–Є—П –њ—А–Є–≤–µ–і–µ–љ –љ–Є–ґ–µ) –Є –њ–Њ–Љ–µ—Й–∞—О—В –≤ —Б—Г—И–Є–ї—М–љ—Л–є —И–Ї–∞—Д (30¬∞–°). –Ь–µ–і–ї–µ–љ–љ–Њ –≤—Л—Б—Л—Е–∞—О—Й–Є–є –ґ–µ–ї–∞—В–Є–љ –Њ–±—А–∞–Ј—Г–µ—В —А–Њ–≤–љ—Г—О –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В—М, –Ї –Ї–Њ—В–Њ—А–Њ–є —Е–Њ—А–Њ—И–Њ –±—Г–і—Г—В –њ—А–Є–Ї—А–µ–њ–ї—П—В—М—Б—П —Б—А–µ–Ј—Л —В–Ї–∞–љ–Є –Љ–Њ–Ј–≥–∞.
–Ф–ї—П –њ—А–Є–≥–Њ—В–Њ–≤–ї–µ–љ–Є—П –ґ–µ–ї–∞—В–Є–љ–∞ –њ–Њ—А–Њ—И–Ї–Њ–Њ–±—А–∞–Ј–љ—Л–є –ґ–µ–ї–∞—В–Є–љ —Б–Љ–µ—И–Є–≤–∞—О—В —Б –і–Є—Б—В–Є–ї–ї–Є—А–Њ–≤–∞–љ–љ–Њ–є –≤–Њ–і–Њ–є –Є –њ–Њ–Љ–µ—Й–∞—О—В –≤ —Б—Г—И–Є–ї—М–љ—Л–є —И–Ї–∞—Д –њ—А–Є 62¬∞–° –Є–ї–Є –≤ –≤–Њ–і—П–љ—Г—О –±–∞–љ—О, —З—В–Њ–±—Л –Њ–љ —А–∞—Б—В–≤–Њ—А–Є–ї—Б—П. –Ъ —А–∞—Б—В–≤–Њ—А—Г –ґ–µ–ї–∞—В–Є–љ–∞ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –і–Њ–±–∞–≤–Є—В—М —Е—А–Њ–Љ–Њ–≤—Л–µ –Ї–≤–∞—Б—Ж—Л. –Ч–∞—В–µ–Љ —Б–Љ–µ—Б—М –љ—Г–ґ–љ–Њ –і–≤–∞–ґ–і—Л –њ—А–Њ—Д–Є–ї—М—В—А–Њ–≤–∞—В—М; –і–ї—П –±—Л—Б—В—А–Њ–є —Д–Є–ї—М—В—А–∞—Ж–Є–Є –ґ–Є–і–Ї–Њ—Б—В–Є –љ–∞–≥—А–µ–є—В–µ –∞–њ–њ–∞—А–∞—В—Г—А—Г –њ–µ—А–µ–і –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –Є –і–µ—А–ґ–Є—В–µ –Ї–Њ–ї–±—Г –љ–∞ –≥–Њ—А—П—З–µ–є –њ–ї–Є—В–µ –Є–ї–Є –≤ –≤–Њ–і—П–љ–Њ–є –±–∞–љ–µ (50¬∞–°). –Я—А–Њ—Д–Є–ї—М—В—А–Њ–≤–∞–љ–љ—Л–є –ґ–µ–ї–∞—В–Є–љ –≥–Њ—В–Њ–≤ –Ї —Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є—О.
–Х—Б—В—М –µ—Й–µ –Њ–і–Є–љ –ї–µ–≥–Ї–Є–є –Є –±—Л—Б—В—А—Л–є —Б–њ–Њ—Б–Њ–± –њ–Њ–Ї—А—Л—В–Є—П –њ—А–µ–і–Љ–µ—В–љ—Л—Е —Б—В–µ–Ї–Њ–ї –ґ–µ–ї–∞—В–Є–љ–Њ–Љ. –†–∞—Б—В–≤–Њ—А–Є—В–µ 0,5 –≥ –ґ–µ–ї–∞—В–Є–љ–∞ –Є 0,05 –≥ —Б—Г–ї—М—Д–∞—В–∞ —Е—А–Њ–Љ–Є—Б—В–Њ–≥–Њ (III) –Ї–∞–ї–Є—П –≤ 100 –Љ–ї –і–Є—Б—В–Є–ї–ї–Є—А–Њ–≤–∞–љ–љ–Њ–є –≤–Њ–і—Л –њ—А–Є 60-70¬∞–°. –Я–Њ–≥—А—Г–Ј–Є—В–µ –њ–Њ–і–љ–Њ—Б —Б–Њ —Б—В–µ–Ї–ї–∞–Љ–Є –≤ —Н—В–Њ—В —А–∞—Б—В–≤–Њ—А –љ–∞ 20 —Б, –∞ –Ј–∞—В–µ–Љ –і–∞–є—В–µ –Є–Љ –≤—Л—Б–Њ—Е–љ—Г—В—М. –Я–Њ—Б–ї–µ —Б—Г—И–Ї–Є –≤ —В–µ—А–Љ–Њ—Б—В–∞—В–µ (40¬∞–°) –њ—А–µ–і–Љ–µ—В–љ—Л–µ —Б—В–µ–Ї–ї–∞ –Љ–Њ–ґ–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М.
–Ь–Ю–Э–Ґ–Ш–†–Ю–Т–Р–Э–Ш–Х –°–†–Х–Ч–Ю–Т
–Ь–∞—В–µ—А–Є–∞–ї—Л. –Ь–µ–ї–Ї–∞—П —З–∞—И–Ї–∞ –Є –љ–µ–±–Њ–ї—М—И–∞—П –Ї–Є—Б—В–Њ—З–Ї–∞ —Б –Ј–∞–Њ—Б—В—А–µ–љ–љ—Л–Љ –Ї–Њ–љ—З–Є–Ї–Њ–Љ.
–Я–µ—А–µ–љ–Њ—Б —Б—А–µ–Ј–Њ–≤ –Љ–Њ–Ј–≥–∞ –љ–∞ –њ—А–µ–і–Љ–µ—В–љ—Л–µ —Б—В–µ–Ї–ї–∞ —В—А–µ–±—Г–µ—В –љ–µ–Ї–Њ—В–Њ—А–Њ–≥–Њ –љ–∞–≤—Л–Ї–∞. –°—А–µ–Ј—Л –Љ–Њ–ґ–љ–Њ –ї–µ–≥–Ї–Њ –њ–µ—А–µ–љ–µ—Б—В–Є –Є–Ј –Њ–і–љ–Њ–≥–Њ —А–∞—Б—В–≤–Њ—А–∞ –≤ –і—А—Г–≥–Њ–є —Б –њ–Њ–Љ–Њ—Й—М—О –Ї–Є—Б—В–Њ—З–Ї–Є. –Я–Њ–Љ–µ—Б—В–Є—В–µ —Б—А–µ–Ј (–Ї–Њ—В–Њ—А—Л–є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –љ–∞—В—П–љ—Г—В—М) –≤ –Љ–µ–ї–Ї—Г—О —З–∞—И–Ї—Г, –љ–∞–њ–Њ–ї–љ–µ–љ–љ—Г—О 0,5вАФ1%-–љ—Л–Љ —Д–Њ—А–Љ–∞–ї–Є–љ–Њ–Љ –Є–ї–Є –≤–Њ–і–Њ–є. –Я–Њ–ї–Њ–ґ–Є–≤ –њ–Њ–Ї—А—Л—В–Њ–µ –ґ–µ–ї–∞—В–Є–љ–Њ–Љ –њ—А–µ–і–Љ–µ—В–љ–Њ–µ —Б—В–µ–Ї–ї–Њ –њ–Њ–і —В–Ї–∞–љ—М, –Њ—Б—В–Њ—А–Њ–ґ–љ–Њ –Є —В—Й–∞—В–µ–ї—М–љ–Њ –љ–∞—В—П–≥–Є–≤–∞–є—В–µ –љ–∞ –љ–µ–≥–Њ —Б—А–µ–Ј. –Р–Ї–Ї—Г—А–∞—В–љ–Њ –њ—А–Є–Ї–Њ—Б–љ–Є—В–µ—Б—М –Ї —В–Ї–∞–љ–Є –Ї–Є—Б—В–Њ—З–Ї–Њ–є, –Љ–µ–і–ї–µ–љ–љ–Њ —Г–і–∞–ї—П—П –≤–Њ–і—Г —Б–Њ —Б—В–µ–Ї–ї–∞. –Ґ–Ї–∞–љ—М –њ—А–Є–Ї–ї–µ–Є—В—Б—П –Ї –ґ–µ–ї–∞—В–Є–љ—Г. –Э–µ –Љ–µ–љ—П–є—В–µ –њ–Њ–ї–Њ–ґ–µ–љ–Є–µ —Б—А–µ–Ј–∞ –Љ–Њ–Ј–≥–∞ –њ–Њ—Б–ї–µ —Г–і–∞–ї–µ–љ–Є—П –≤–Њ–і—Л. –°—В–∞—А–∞–є—В–µ—Б—М –љ–µ –љ–∞–Љ–Њ—З–Є—В—М —Г–ґ–µ –њ—А–Є–Ї–ї–µ–µ–љ–љ—Л–є —Б—А–µ–Ј –њ—А–Є –љ–∞—В—П–≥–Є–≤–∞–љ–Є–Є —Б–ї–µ–і—Г—О—Й–µ–≥–Њ —Б—А–µ–Ј–∞.
–Х—Б–ї–Є —Б—В–µ–Ї–ї–∞ –њ–Њ–Ї—А—Л–≤–∞–ї–Є –ґ–µ–ї–∞—В–Є–љ–Њ–Љ –њ–Њ –≤—В–Њ—А–Њ–Љ—Г —Б–њ–Њ—Б–Њ–±—Г (–ґ–µ–ї–∞—В–Є–љ –њ–ї—О—Б —Б—Г–ї—М—Д–∞—В —Е—А–Њ–Љ–Є—Б—В–Њ–≥–Њ –Ї–∞–ї–Є—П), —В–Њ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ—А–Є–≥–Њ—В–Њ–≤–Є—В—М –ґ–µ–ї–∞—В–Є–љ –і–ї—П –Љ–Њ–љ—В–Є—А–Њ–≤–∞–љ–Є—П —Б—А–µ–Ј–Њ–≤.
–Ф–ї—П —Н—В–Є—Е —Ж–µ–ї–µ–є —А–∞—Б—В–≤–Њ—А–Є—В–µ 0,75 –≥ –ґ–µ–ї–∞—В–Є–љ–∞ –≤ 40 –Љ–ї –і–Є—Б—В–Є–ї–ї–Є—А–Њ–≤–∞–љ–љ–Њ–є –Э2–Ю –њ—А–Є 60вАФ70¬∞–°. –Ч–∞—В–µ–Љ –і–Њ–±–∞–≤—М—В–µ 20 –Љ–ї –і–Є—Б—В–Є–ї–ї–Є—А–Њ–≤–∞–љ–љ–Њ–є –≤–Њ–і—Л –Є 40 –Љ–ї —З–Є—Б—В–Њ–≥–Њ —Н—В–∞–љ–Њ–ї–∞. –≠—В–Њ—В —А–∞—Б—В–≤–Њ—А –љ—Г–ґ–љ–Њ —Е—А–∞–љ–Є—В—М –≤ —Е–Њ–ї–Њ–і–Є–ї—М–љ–Є–Ї–µ. –І—В–Њ–±—Л –љ–∞—В—П–љ—Г—В—М —Б—А–µ–Ј—Л, —Б–љ–∞—З–∞–ї–∞ –њ–Њ–Љ–µ—Б—В–Є—В–µ –Є—Е –≤ —З–∞—И–Ї—Г –Я–µ—В—А–Є —Б –њ–Њ–і–Њ–≥—А–µ—В—Л–Љ –љ–∞ —В–µ–њ–ї–Њ–є –њ–ї–Є—В–Ї–µ –ґ–µ–ї–∞—В–Є–љ–Њ–Љ (–і–Њ 35¬∞–°).
–Я–Њ—Б–ї–µ –Љ–Њ–љ—В–Є—А–Њ–≤–∞–љ–Є—П —Б—А–µ–Ј–Њ–≤ –њ—А–µ–і–Љ–µ—В–љ—Л–µ —Б—В–µ–Ї–ї–∞ –Љ–∞—А–Ї–Є—А—Г—О—В —Б –њ–Њ–Љ–Њ—Й—М—О —Б—В–µ–Ї–ї–Њ–≥—А–∞—Д–∞.
–§–Ю–Ґ–Ю–У–†–Р–§–Ш–†–Ю–Т–Р–Э–Ш–Х –Э–Х–Ю–Ъ–†–Р–®–Х–Э–Э–Ђ–• –°–†–Х–Ч–Ю–Т
–Э–∞ —Н—В–Њ–є —Б—В–∞–і–Є–Є –њ—А–Њ—Б—В—Г—О –≥–Є—Б—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї—Г—О –Њ—Ж–µ–љ–Ї—Г –Љ–Њ–ґ–љ–Њ –Њ—Б—Г—Й–µ—Б—В–≤–Є—В—М, –њ–Њ–Љ–µ—Й–∞—П –Љ–Њ–љ—В–Є—А–Њ–≤–∞–љ–љ—Л–є —Б—А–µ–Ј –њ–Њ–і —Ж–Є—Д—А–Њ–≤–Њ–є —Д–Њ—В–Њ–∞–њ–њ–∞—А–∞—В —Г–Ї—А–µ–њ–ї–µ–љ–љ—Л–є –љ–∞ —И—В–∞—В–Є–≤–µ. –°–Љ–Њ—З–Є—В–µ —Б—А–µ–Ј –≥–ї–Є—Ж–µ—А–Є–љ–Њ–Љ. –Я–Њ–Ј–Є—В–Є–≤–љ—Л–є –Њ—В–њ–µ—З–∞—В–Њ–Ї –≤—Л—П–≤–ї—П–µ—В –Љ–Є–µ–ї–Є–љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–µ –≤–Њ–ї–Њ–Ї–љ–∞, –љ–Њ –љ–µ —П–і—А–∞ —Б–µ—А–Њ–≥–Њ –≤–µ—Й–µ—Б—В–≤–∞. –Х—Б–ї–Є –Љ–Њ–Ј–≥ –±—Л–ї –њ—А–∞–≤–Є–ї—М–љ–Њ —А–∞–Ј—А–µ–Ј–∞–љ –љ–∞ –±–ї–Њ–Ї–Є, —В–Њ —В–∞–Ї–Є—Е —Д–Њ—В–Њ–≥—А–∞—Д–Є–є –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –і–ї—П –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П –њ—Г—В–µ–Љ —Б—А–∞–≤–љ–µ–љ–Є—П —Б —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–µ–є –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–є –њ–ї–Њ—Б–Ї–Њ—Б—В—М—О –љ–∞ –∞—В–ї–∞—Б–µ. –У—А—Г–±–∞—П —А–µ–Ї–Њ–љ—Б—В—А—Г–Ї—Ж–Є—П –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–є –і–Њ—Б—В–Є–≥–∞–µ—В—Б—П —Б –њ–Њ–Љ–Њ—Й—М—О —Б–Њ–њ–Њ—Б—В–∞–≤–ї–µ–љ–Є–є —Д–Њ—В–Њ–≥—А–∞—Д–Є–є —Б –∞—В–ї–∞—Б–Њ–Љ.
–Ю–Ъ–†–Р–®–Ш–Т–Р–Э–Ш–Х
–Э–Є–ґ–µ –Њ–њ–Є—Б—Л–≤–∞–µ—В—Б—П –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –Љ–µ—В–Њ–і–Њ–≤ –Њ–Ї—А–∞—И–Є–≤–∞–љ–Є—П. –Я–Њ —Н—В–Є–Љ –Љ–µ—В–Њ–і–Є–Ї–∞–Љ —Б—А–µ–Ј—Л –Њ–±—Л—З–љ–Њ –Љ–Њ–љ—В–Є—А—Г—О—В—Б—П –љ–∞ –њ–Њ–Ї—А—Л—В—Л–µ –ґ–µ–ї–∞—В–Є–љ–Њ–Љ –њ—А–µ–і–Љ–µ—В–љ—Л–µ —Б—В–µ–Ї–ї–∞ –Є –≤—Л—Б—Г—И–Є–≤–∞—О—В—Б—П –њ–µ—А–µ–і –Њ–Ї—А–∞—И–Є–≤–∞–љ–Є–µ–Љ.
1. –Ю–Ї—А–∞—И–Є–≤–∞–љ–Є–µ –Ї—А–µ–Ј–Є–ї–≤–Є–Њ–ї–µ—В–Њ–Љ
–Ф–ї—П –њ—А–Є–≥–Њ—В–Њ–≤–ї–µ–љ–Є—П —Н—В–Њ–≥–Њ –Ї—А–∞—Б–Є—В–µ–ї—П —А–∞—Б—В–≤–Њ—А–Є—В–µ 0,25вАФ0,5 –≥ –Ї—А–µ–Ј–Є–ї–≤–Є–Њ–ї–µ—В–∞ –≤ 100 –Љ–ї –і–Є—Б—В–Є–ї–ї–Є—А–Њ–≤–∞–љ–љ–Њ–є –≤–Њ–і—Л.
–Я—А–Є–≥–Њ—В–Њ–≤–ї–µ–љ–љ—Л–є —А–∞—Б—В–≤–Њ—А –њ–µ—А–µ–Љ–µ—И–Є–≤–∞—О—В, —Д–Є–ї—М—В—А—Г—О—В –Є —Е—А–∞–љ—П—В –≤ —В–µ–Љ–љ–Њ–Љ —Б–Њ—Б—Г–і–µ –њ—А–Є –Ї–Њ–Љ–љ–∞—В–љ–Њ–є —В–µ–Љ–њ–µ—А–∞—В—Г—А–µ. –†–∞—Б—В–≤–Њ—А –Љ–Њ–ґ–µ—В —Е—А–∞–љ–Є—В—М—Б—П –љ–µ–Њ–≥—А–∞–љ–Є—З–µ–љ–љ–Њ–µ –≤—А–µ–Љ—П.
–Я–µ—А–µ–і –Њ–Ї—А–∞—И–Є–≤–∞–љ–Є–µ–Љ —Б—А–µ–Ј—Л –Њ–±–µ–Ј–≤–Њ–ґ–Є–≤–∞—О—В –њ—Г—В–µ–Љ –Є–љ–Ї—Г–±–∞—Ж–Є–Є –≤ 50%-–љ–Њ–Љ —Н—В–∞–љ–Њ–ї–µ, –Ј–∞—В–µ–Љ –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ –≤ 70, 96 –Є 100%-–љ–Њ–Љ —Н—В–∞–љ–Њ–ї–µ, –≤ –Ї–∞–ґ–і–Њ–Љ —Б–ї—Г—З–∞–µ –≤ —В–µ—З–µ–љ–Є–µ 10 –Љ–Є–љ. –Я–Њ—В–Њ–Љ —Б—А–µ–Ј—Л –њ–Њ–Љ–µ—Й–∞—О—В –≤ –Ї—Б–Є–ї–Њ–ї –љ–∞ 1вАФ2 —З, –≥–і–µ –Є—Е –Љ–Њ–ґ–љ–Њ –і–∞–ґ–µ –Њ—Б—В–∞–≤–Є—В—М –љ–∞ –љ–Њ—З—М. –Я–Њ—Б–ї–µ —Н—В–Њ–≥–Њ —Б—А–µ–Ј—Л –≤–љ–Њ–≤—М –Њ–±–µ–Ј–≤–Њ–ґ–Є–≤–∞—О—В, –њ–Њ–Љ–µ—Й–∞—П –≤ 96, 70 –Є 50%- –љ—Л–µ —А–∞—Б—В–≤–Њ—А—Л —Н—В–∞–љ–Њ–ї–∞ (2вАФ5 –Љ–Є–љ –≤ –Ї–∞–ґ–і–Њ–Љ —А–∞—Б—В–≤–Њ—А–µ), –∞ –Ј–∞—В–µ–Љ –≤ –і–Є—Б—В–Є–ї–ї–Є—А–Њ–≤–∞–љ–љ—Г—О –≤–Њ–і—Г (5 –Љ–Є–љ). –°—А–µ–Ј—Л –њ–Њ–≥—А—Г–ґ–∞—О—В –≤ —А–∞—Б—В–≤–Њ—А –Ї—А–µ–Ј–Є–ї–≤–Є–Њ–ї–µ—В–∞ –љ–∞ 15вАФ60 —Б. –Ч–∞—В–µ–Љ –Є—Е –њ—А–Њ–Љ—Л–≤–∞—О—В –≤ –і–Є—Б—В–Є–ї–ї–Є—А–Њ–≤–∞–љ–љ–Њ–є –≤–Њ–і–µ –Є –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А—Г—О—В –≤ –њ–Њ–і–Ї–Є—Б–ї–µ–љ–љ–Њ–Љ —Б–њ–Є—А—В–µ (—А–∞—Б—В–≤–Њ—А, —Б–Њ—Б—В–Њ—П—Й–Є–є –Є–Ј 96%-–љ–Њ–≥–Њ —Н—В–∞–љ–Њ–ї–∞ —Б –і–Њ–±–∞–≤–ї–µ–љ–Є–µ–Љ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –Ї–∞–њ–µ–ї—М —Г–Ї—Б—Г—Б–љ–Њ–є –Ї–Є—Б–ї–Њ—В—Л). –Я–Њ—Б–ї–µ –і–≤—Г—Е —Б–Љ–µ–љ —А–∞—Б—В–≤–Њ—А–∞ —Н—В–∞–љ–Њ–ї–∞ —Б—А–µ–Ј—Л –њ—А–Њ—Б–≤–µ—В–ї—П—О—В –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ –≤ –і–≤—Г—Е –њ–Њ—А—Ж–Є—П—Е –Ї—Б–Є–ї–Њ–ї–∞ –Є –Ј–∞–Ї–ї—О—З–∞—О—В –њ–Њ–і –њ–Њ–Ї—А–Њ–≤–љ—Л–µ —Б—В–µ–Ї–ї–∞. –Ф–ї—П —Н—В–Њ–≥–Њ –≤—Л–љ–Є–Љ–∞—О—В –њ—А–µ–і–Љ–µ—В–љ–Њ–µ —Б—В–µ–Ї–ї–Њ –Є–Ј –Ї—Б–Є–ї–Њ–ї–∞ –Є –і–∞—О—В –µ–Љ—Г –≤—Л—Б–Њ—Е–љ—Г—В—М –≤ —В–µ—З–µ–љ–Є–µ 10 —Б, –Ј–∞—В–µ–Љ –љ–∞–љ–Њ—Б—П—В –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –Ї–∞–њ–µ–ї—М –Ї–∞–љ–∞–і—Б–Ї–Њ–≥–Њ –±–∞–ї—М–Ј–∞–Љ–∞ –љ–∞ —В—Г —Б—В–Њ—А–Њ–љ—Г —Б—В–µ–Ї–ї–∞, –≥–і–µ —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ—Л —Б—А–µ–Ј—Л, –Є –љ–∞–Ї—А—Л–≤–∞—О—В —Б–≤–µ—А—Е—Г –њ–Њ–Ї—А–Њ–≤–љ—Л–Љ —Б—В–µ–Ї–ї–Њ–Љ. –°–ї–µ–і—Г–µ—В –њ–Њ–Ј–∞–±–Њ—В–Є—В—М—Б—П –Њ —В–Њ–Љ, —З—В–Њ–±—Л –љ–µ –±—Л–ї–Њ –њ—Г–Ј—Л—А—М–Ї–Њ–≤ –≤–Њ–Ј–і—Г—Е–∞. –°—В–µ–Ї–ї–∞–Љ –і–∞—О—В –≤—Л—Б–Њ—Е–љ—Г—В—М. –†–∞—Б—В–≤–Њ—А –Ї—А–µ–Ј–Є–ї–≤–Є–Њ–ї–µ—В–∞ –Љ–Њ–ґ–µ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М—Б—П –і–ї—П –Є–і–µ–љ—В–Є—Д–Є–Ї–∞—Ж–Є–Є –і–µ–≥–µ–љ–µ—А–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–Ї–∞–љ–Є –Љ–Њ–Ј–≥–∞: –Њ–љ –Њ–Ї—А–∞—И–Є–≤–∞–µ—В –≤–µ—Й–µ—Б—В–≤–Њ –Э–Є—Б—Б–ї—П –Є–љ—В–∞–Ї—В–љ—Л—Е –љ–µ–є—А–Њ–љ–Њ–≤ –≤ —Б–Є–љ–Є–є —Ж–≤–µ—В.
–Ю —Е—А–Њ–Љ–∞—В–Њ–ї–Є–Ј–µ, –љ–∞–±—Г—Е–∞–љ–Є–Є –њ–µ—А–Є–Ї–∞—А–Є–Њ–љ–∞ –Є —Н–Ї—Б—Ж–µ–љ—В—А–Є—З–љ–Њ—Б—В–Є —П–і—А–∞ –і–µ–≥–µ–љ–µ—А–Є—А—Г—О—Й–Є—Е –љ–µ–є—А–Њ–љ–Њ–≤ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В —А–∞–Ј–Љ—Л—В—Л–µ –Ј–Њ–љ—Л –≤ –љ–µ—А–≤–љ–Њ–є —В–Ї–∞–љ–Є.
2. –Э–µ–є—В—А–∞–ї—М–љ—Л–є –Ї—А–∞—Б–љ—Л–є
–Ф–ї—П –њ—А–Є–≥–Њ—В–Њ–≤–ї–µ–љ–Є—П —Н—В–Њ–≥–Њ –Ї—А–∞—Б–Є—В–µ–ї—П 1 –≥ –љ–µ–є—В—А–∞–ї—М–љ–Њ–≥–Њ –Ї—А–∞—Б–љ–Њ–≥–Њ —А–∞—Б—В–≤–Њ—А—П—О—В –≤ 100 –Љ–ї –і–Є—Б—В–Є–ї–ї–Є—А–Њ–≤–∞–љ–љ–Њ–є –≤–Њ–і—Л. –Ч–∞—В–µ–Љ —В—Г–і–∞ –і–Њ–±–∞–≤–ї—П—О—В 4 –Љ–ї –∞—Ж–µ—В–∞—В–љ–Њ–≥–Њ –±—Г—Д–µ—А–∞ (pH 4,8). –Р—Ж–µ—В–∞—В–љ—Л–є –±—Г—Д–µ—А —Б–Њ—Б—В–Њ–Є—В –Є–Ј 500 –Љ–ї 0,1 N —Г–Ї—Б—Г—Б–љ–Њ–є –Ї–Є—Б–ї–Њ—В—Л, —Б–Љ–µ—И–∞–љ–љ–Њ–є —Б 750 –Љ–ї 0,1 N –∞—Ж–µ—В–∞—В–∞ –љ–∞—В—А–Є—П. –Я–µ—А–µ–і –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —А–∞—Б—В–≤–Њ—А –љ—Г–ґ–љ–Њ –њ—А–Њ—Д–Є–ї—М—В—А–Њ–≤–∞—В—М, –Ї—А–Њ–Љ–µ —В–Њ–≥–Њ, –µ–≥–Њ –Љ–Њ–ґ–љ–Њ –њ–Њ–і–Њ–≥—А–µ—В—М –і–ї—П —Г–ї—Г—З—И–µ–љ–Є—П –Њ–Ї—А–∞—И–Є–≤–∞–љ–Є—П –≥–ї—Л–±–Њ–Ї –Э–Є—Б—Б–ї—П. –Ю–љ–Є –Є–Љ–µ—О—В –Њ—А–∞–љ–ґ–µ–≤–Њ-–Ї—А–∞—Б–љ—Г—О –Њ–Ї—А–∞—Б–Ї—Г –Є –≤—Л–і–µ–ї—П—О—В—Б—П –љ–∞ –±–ї–µ–і–љ–Њ–Љ —Б–≤–µ—В–ї–Њ-–Њ—А–∞–љ–ґ–µ–≤–Њ-–Ї–Њ—А–Є—З–љ–µ–≤–Њ–Љ —Д–Њ–љ–µ.
–Ъ–Њ–≥–і–∞ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В –Ї—А–µ–Ј–Є–ї–≤–Є–Њ–ї–µ—В –Є–ї–Є –љ–µ–є—В—А–∞–ї—М–љ—Л–є –Ї—А–∞—Б–љ—Л–є, —В–Њ –њ–µ—А–µ–і –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–Ї–Њ–є –≤ 96%-–љ–Њ–Љ —Б–њ–Є—А—В–µ –Љ–Њ–ґ–љ–Њ –њ—А–Њ–Є–Ј–≤–µ—Б—В–Є –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –Ї–Њ—А–Њ—В–Ї–Є—Е –Є–љ–Ї—Г–±–∞—Ж–Є–є (1 –Љ–Є–љ –љ–∞ –Ї–∞–ґ–і—Г—О –Є–љ–Ї—Г–±–∞—Ж–Є—О) —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ –≤ 50, 70 –Є 96%-–љ–Њ–Љ —Н—В–∞–љ–Њ–ї–µ. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ –њ–µ—А–µ–і –њ–Њ–Љ–µ—Й–µ–љ–Є–µ–Љ —Б—А–µ–Ј–Њ–≤ –≤ –Ї—Б–Є–ї–Њ–ї –Є—Е –Љ–Њ–ґ–љ–Њ –Ї–Њ—А–Њ—В–Ї–Њ–µ –≤—А–µ–Љ—П –≤—Л–і–µ—А–ґ–∞—В—М –≤ —Б–Љ–µ—Б–Є –Є–Ј —А–∞–≤–љ—Л—Е —З–∞—Б—В–µ–є 96%-–љ–Њ–≥–Њ —Н—В–∞–љ–Њ–ї–∞ –Є –Ї—Б–Є–ї–Њ–ї–∞.
–†–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –њ–µ—А–µ–і —В–µ–Љ –Ї–∞–Ї –љ–∞–Ї—А—Л—В—М —Б—А–µ–Ј—Л –њ–Њ–Ї—А–Њ–≤–љ—Л–Љ —Б—В–µ–Ї–ї–Њ–Љ, –Ї—Б–Є–ї–Њ–ї –Њ–±–љ–Њ–≤–ї—П—В—М –і–≤–∞ —А–∞–Ј–∞. –Т –њ–Њ—Б–ї–µ–і–љ–µ–є –њ–Њ—А—Ж–Є–Є —Б—А–µ–Ј—Л –і–Њ–ї–ґ–љ—Л –љ–∞—Е–Њ–і–Є—В—М—Б—П –љ–µ –Љ–µ–љ–µ–µ 5 –Љ–Є–љ.
3. –Ю–Ї—А–∞—И–Є–≤–∞–љ–Є–µ –њ–Њ –Љ–µ—В–Њ–і—Г –Ъ–ї—О–≤–µ—А-–С–∞—А—А–µ—А–∞
–Ъ–∞–Ї –љ–µ–є—В—А–∞–ї—М–љ—Л–є –Ї—А–∞—Б–љ—Л–є, —В–∞–Ї –Є –Ї—А–µ–Ј–Є–ї–≤–Є–Њ–ї–µ—В –Љ–Њ–ґ–љ–Њ —Б–Њ—З–µ—В–∞—В—М —Б –Њ–Ї—А–∞—И–Є–≤–∞–љ–Є–µ–Љ –±—Л—Б—В—А—Л–Љ –≥–Њ–ї—Г–±—Л–Љ –ї—О–Ї—Б–Њ–ї–µ–Љ –Љ–Є–µ–ї–Є–љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ (KluverвАФBarrera, 1963; Lockard and Reers, 1962) –і–ї—П –Њ–Ї—А–∞—И–Є–≤–∞–љ–Є—П –њ–Њ –Љ–µ—В–Њ–і—Г –Ъ–ї—О–≤–µ—АвАФ–С–∞—А—А–µ—А–∞.
–Ф–ї—П –њ—А–Є–≥–Њ—В–Њ–≤–ї–µ–љ–Є—П 0,1%-–љ–Њ–≥–Њ —А–∞—Б—В–≤–Њ—А–∞ –±—Л—Б—В—А–Њ–≥–Њ –≥–Њ–ї—Г–±–Њ–≥–Њ –ї—О–Ї—Б–Њ–ї—П 1 –≥ –Ї—А–∞—Б–Є—В–µ–ї—П —А–∞—Б—В–≤–Њ—А—П—О—В –≤ 1000 –Љ–ї 96%-–љ–Њ–≥–Њ —Н—В–∞–љ–Њ–ї–∞; –Ј–∞—В–µ–Љ –і–Њ–±–∞–≤–ї—П—О—В 5 –Љ–ї 10%-–љ–Њ–є —Г–Ї—Б—Г—Б–љ–Њ–є –Ї–Є—Б–ї–Њ—В—Л. –†–∞—Б—В–≤–Њ—А –њ–µ—А–µ–Љ–µ—И–Є–≤–∞—О—В, —Д–Є–ї—М—В—А—Г—О—В –Є –≤—Л–і–µ—А–ґ–Є–≤–∞—О—В –њ–µ—А–µ–і –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –≤ —В–µ—З–µ–љ–Є–µ 24 —З. –†–∞—Б—В–≤–Њ—А —Е—А–∞–љ–Є—В—Б—П –љ–µ–Њ–≥—А–∞–љ–Є—З–µ–љ–љ–Њ–µ –≤—А–µ–Љ—П.
–Ф–ї—П –Њ–Ї—А–∞—И–Є–≤–∞–љ–Є—П —Б –њ–Њ–Љ–Њ—Й—М—О –±—Л—Б—В—А–Њ–≥–Њ –≥–Њ–ї—Г–±–Њ–≥–Њ –ї—О–Ї—Б–Њ–ї—П —Б—А–µ–Ј—Л –њ—А–µ–і–≤–∞—А–Є—В–µ–ї—М–љ–Њ –≤—Л–і–µ—А–ґ–Є–≤–∞—О—В –≤ 96%-–љ–Њ–Љ —Н—В–∞–љ–Њ–ї–µ –≤ —В–µ—З–µ–љ–Є–µ 10 –Љ–Є–љ, –∞ –Ј–∞—В–µ–Љ –њ–µ—А–µ–љ–Њ—Б—П—В –≤ —А–∞—Б—В–≤–Њ—А –±—Л—Б—В—А–Њ–≥–Њ –≥–Њ–ї—Г–±–Њ–≥–Њ –ї—О–Ї—Б–Њ–ї—П –Є –њ–Њ–Љ–µ—Й–∞—О—В –љ–∞ 2вАФ4 —З –≤ —В–µ—А–Љ–Њ—Б—В–∞—В –њ—А–Є 56¬∞–°. –Ъ–Њ–≥–і–∞ –Њ–Ї—А–∞—И–Є–≤–∞–љ–Є–µ –Ј–∞–≤–µ—А—И–µ–љ–Њ, –≤–Њ–ї–Њ–Ї–љ–∞ –Є–Љ–µ—О—В —В–µ–Љ–љ–Њ-—Б–Є–љ–Є–є, –∞ –Ї–ї–µ—В–Ї–Є вАФ —Б–≤–µ—В–ї–Њ- —Б–Є–љ–Є–є —Ж–≤–µ—В. –°—А–µ–Ј—Л –Њ—Б–≤–µ—В–ї—П—О—В –≤ 96%-–љ–Њ–Љ —Н—В–∞–љ–Њ–ї–µ, –Ј–∞—В–µ–Љ —Б–њ–Њ–ї–∞—Б–Ї–Є–≤–∞—О—В –≤ –і–Є—Б—В–Є–ї–ї–Є—А–Њ–≤–∞–љ–љ–Њ–є –≤–Њ–і–µ –Є –њ–Њ–Љ–µ—Й–∞—О—В –≤ 0,05%-–љ—Л–є –≤–Њ–і–љ—Л–є —А–∞—Б—В–≤–Њ—А –Ї–∞—А–±–Њ–љ–∞—В–∞ –ї–Є—В–Є—П –љ–∞ 5 –Љ–Є–љ.
–Я–Њ—Б–ї–µ–і–љ–Є–є –њ—А–Є–≥–Њ—В–Њ–≤–ї—П–µ—В—Б—П –Є–Ј 0,5 –≥ –Ї–∞—А–±–Њ–љ–∞—В–∞ –ї–Є—В–Є—П, —А–∞—Б—В–≤–Њ—А–µ–љ–љ–Њ–≥–Њ –≤ 1000 –Љ–ї –і–Є—Б—В–Є–ї–ї–Є—А–Њ–≤–∞–љ–љ–Њ–є –≤–Њ–і—Л.
–°—А–µ–Ј—Л –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А—Г—О—В –≤ 70%-–љ–Њ–Љ —Н—В–∞–љ–Њ–ї–µ –≤ —В–µ—З–µ–љ–Є–µ 1вАФ3 –Љ–Є–љ –Є –њ—А–Њ–Љ—Л–≤–∞—О—В –і–Є—Б—В–Є–ї–ї–Є—А–Њ–≤–∞–љ–љ–Њ–є –≤–Њ–і–Њ–є. –Я–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ–µ –њ—А–Њ–Љ—Л–≤–∞–љ–Є–µ –≤ –Ї–∞—А–±–Њ–љ–∞—В–µ –ї–Є—В–Є—П –Є 70%-–љ–Њ–Љ —Н—В–∞–љ–Њ–ї–µ –Љ–Њ–ґ–љ–Њ –њ–Њ–≤—В–Њ—А–Є—В—М –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —А–∞–Ј, –µ—Б–ї–Є –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–Ї–∞ –Њ–Ї–∞–Ј–∞–ї–∞—Б—М –љ–µ—Г–і–Њ–≤–ї–µ—В–≤–Њ—А–Є—В–µ–ї—М–љ–Њ–є.
–Ґ–µ–њ–µ—А—М —Б—А–µ–Ј—Л –Љ–Њ–ґ–љ–Њ –њ–Њ–і–Ї—А–∞—Б–Є—В—М –Ї—А–µ–Ј–Є–ї–≤–Є–Њ–ї–µ—В–Њ–Љ (6вАФ10 –Љ–Є–љ) –Є–ї–Є –љ–µ–є—В—А–∞–ї—М–љ—Л–Љ- –Ї—А–∞—Б–љ—Л–Љ (2вАФ4 –Љ–Є–љ) —Б–Њ–≥–ї–∞—Б–љ–Њ —Г–ґ–µ –Њ–њ–Є—Б–∞–љ–љ—Л–Љ –њ—А–Њ—Ж–µ–і—Г—А–∞–Љ. –Ю–і–љ–∞–Ї–Њ —Б–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ —Б—А–µ–Ј—Л –≤—Л–і–µ—А–ґ–Є–≤–∞—О—В –≤ –Ї—А–µ–Ј–Є–ї–≤–Є–Њ–ї–µ—В–µ 6вАФ10 –Љ–Є–љ –≤–Љ–µ—Б—В–Њ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е —Б–µ–Ї—Г–љ–і, —В–∞–Ї –Ї–∞–Ї –љ–µ –њ—А–Њ–Є–Ј–≤–Њ–і–Є–ї–∞—Б—М –њ—А–µ–і–≤–∞—А–Є—В–µ–ї—М–љ–∞—П –Є–љ–Ї—Г–±–∞—Ж–Є—П –≤ –Ї—Б–Є–ї–Њ–ї–µ. –Я—А–Є –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–Є–Є –Ї—А–µ–Ј–Є–ї–≤–Є–Њ–ї–µ—В–∞ –Є –±—Л—Б—В—А–Њ–≥–Њ –≥–Њ–ї—Г–±–Њ–≥–Њ –ї—О–Ї—Б–Њ–ї—П —В–µ–ї–∞ –Ї–ї–µ—В–Њ–Ї –Є –Љ–Є–µ–ї–Є–љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–µ –∞–Ї—Б–Њ–љ—Л –Њ–Ї—А–∞—И–Є–≤–∞—О—В—Б—П –≤ –і–≤–∞ —А–∞–Ј–ї–Є—З–љ—Л—Е –Њ—В—В–µ–љ–Ї–∞ —Б–Є–љ–µ–≥–Њ —Ж–≤–µ—В–∞. –Я—А–Є –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–Є–Є –љ–µ–є—В—А–∞–ї—М–љ–Њ–≥–Њ –Ї—А–∞—Б–љ–Њ–≥–Њ –Є –±—Л—Б—В—А–Њ–≥–Њ –≥–Њ–ї—Г–±–Њ–≥–Њ –ї—О–Ї—Б–Њ–ї—П —В–µ–ї–∞ –Ї–ї–µ—В–Њ–Ї –Њ–Ї—А–∞—И–Є–≤–∞—О—В—Б—П –≤ –Њ—А–∞–љ–ґ–µ–≤—Л–є —Ж–≤–µ—В, –∞ –Љ–Є–µ–ї–Є–љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–µ –≤–Њ–ї–Њ–Ї–љ–∞ вАФ –≤ —Б–Є–љ–Є–є.
–Ъ–∞–ґ–і–∞—П –Є–Ј —Н—В–Є—Е –њ—А–Њ—Ж–µ–і—Г—А –Љ–Њ–ґ–µ—В –±—Л—В—М –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–∞ –Њ—В–і–µ–ї—М–љ–Њ –Є–ї–Є –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є (–љ–µ–є—В—А–∞–ї—М–љ—Л–є –Ї—А–∞—Б–љ—Л–є –њ–ї—О—Б –±—Л—Б—В—А—Л–є –≥–Њ–ї—Г–±–Њ–є –ї—О–Ї—Б–Њ–ї—М –Є–ї–Є –Ї—А–µ–Ј–Є–ї–≤–Є–Њ–ї–µ—В –њ–ї—О—Б –±—Л—Б—В—А—Л–є –≥–Њ–ї—Г–±–Њ–є –ї—О–Ї—Б–Њ–ї—М) –і–ї—П –Њ–±—Л—З–љ–Њ–≥–Њ –Њ–Ї—А–∞—И–Є–≤–∞–љ–Є—П –њ–Њ—Б–ї–µ —А–∞–Ј—А—Г—И–µ–љ–Є–є –Љ–Њ–Ј–≥–∞, –≤–ґ–Є–≤–ї–µ–љ–Є—П —Н–ї–µ–Ї—В—А–Њ–і–Њ–≤, –њ–Њ—Б–ї–µ –њ–µ—А–µ—А–µ–Ј–Њ–Ї –Є —В. –і. –С—Л—Б—В—А—Л–є –≥–Њ–ї—Г–±–Њ–є –ї—О–Ї—Б–Њ–ї—М –љ–µ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –њ—А–Њ–Є–Ј–≤–Њ–і–Є—В—М —З–µ—В–Ї—Г—О –і–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞—Ж–Є—О –љ–Њ—А–Љ–∞–ї—М–љ—Л—Е –Є –і–µ–≥–µ–љ–µ—А–Є—А–Њ–≤–∞–љ–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ. –Ф–ї—П —В–∞–Ї–Њ–є –і–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞—Ж–Є–Є –µ—Б—В—М —Б–њ–µ—Ж–Є–∞–ї—М–љ–∞—П –Љ–µ—В–Њ–і–Є–Ї–∞ –Є–Љ–њ—А–µ–≥–љ–Є—А–Њ–≤–∞–љ–Є—П —Б–µ—А–µ–±—А–Њ–Љ.
|