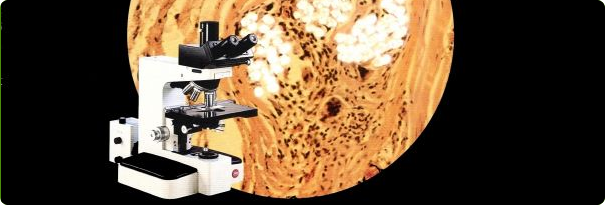
–Я–†–Ю–Ґ–Ю–Ъ–Ю–Ы. –Я—А–Є–≥–Њ—В–Њ–≤–ї–µ–љ–Є–µ —Е—А–Њ–Љ–Њ—Б–Њ–Љ–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞
–°—Е–µ–Љ–∞
–Ч–∞—Д–Є–Ї—Б–Є—А–Њ–≤–∞—В—М –Ї–ї–µ—В–Ї–Є, –±–ї–Њ–Ї–Є—А–Њ–≤–∞–љ–љ—Л–µ –≤ –Љ–µ—В–∞—Д–∞–Ј–µ –Є –љ–∞–±—Г—Е—И–Є–µ –≤ –≥–Є–њ–Њ—В–Њ–љ–Є—З–µ—Б–Ї–Њ–є —Б—А–µ–і–µ. –Ъ–∞–њ–љ—Г—В—М –Ї–ї–µ—В–Ї–Є –љ–∞ —Б—В–µ–Ї–ї–Њ, –Њ–Ї—А–∞—Б–Є—В—М –Є –Є—Б—Б–ї–µ–і–Њ–≤–∞—В—М (—А–Є—Б. 16.6) [Rothfels –Є Siminovitch, 1958; Rooney –Є Czepulkowski, 1986].
–Ь–∞—В–µ—А–Є–∞–ї—Л
–°—В–µ—А–Є–ї—М–љ—Л–µ –Є–ї–Є –∞—Б–µ–њ—В–Є—З–µ—Б–Ї–Є –њ–Њ–і–≥–Њ—В–Њ–≤–ї–µ–љ–љ—Л–µ:
вАҐ –Ъ—Г–ї—М—В—Г—А–∞ –Ї–ї–µ—В–Њ–Ї –≤ log-—Д–∞–Ј–µ
вАҐ –Ъ–Њ–ї—М—Ж–µ–Љ–Є–і, lxlO-5 –Ь –≤ D-PBSA
вАҐ D-PBSA
вАҐ –Ґ—А–Є–њ—Б–Є–љ –љ–µ–Њ—З–Є—Й–µ–љ–љ—Л–є, 0,25%
–Э–µ—Б—В–µ—А–Є–ї—М–љ—Л–µ:
вАҐ –У–Є–њ–Њ—В–Њ–љ–Є—З–µ—Б–Ї–Є–є —А–∞—Б—В–≤–Њ—А: 0,04 –Ь. KCL, 0,025 –Ь —Ж–Є—В—А–∞—В –љ–∞—В—А–Є—П
вАҐ –°–≤–µ–ґ–µ–њ—А–Є–≥–Њ—В–Њ–≤–ї–µ–љ–љ—Л–є —Д–Є–Ї—Б–∞—В–Њ—А (—Г–Ї—Б—Г—Б–љ—Л–є –Љ–µ—В–∞–љ–Њ–ї): 1 —З–∞—Б—В—М –ї–µ–і—П–љ–Њ–є —Г–Ї—Б—Г—Б–љ–Њ–є –Ї–Є—Б–ї–Њ—В—Л –њ–ї—О—Б 3 —З–∞—Б—В–Є –±–µ–Ј–≤–Њ–і–љ–Њ–≥–Њ –Љ–µ—В–∞–љ–Њ–ї–∞ –Є–ї–Є —Н—В–∞–љ–Њ–ї–∞, —Е—А–∞–љ–Є—В—М –љ–∞ –ї—М–і—Г
вАҐ –Ъ—А–∞—Б–Є—В–µ–ї—М –У–Є–Љ–Ј–∞
вАҐ DPX –Є–ї–Є Permount mountant
вАҐ –Ы–µ–і
вАҐ –¶–µ–љ—В—А–Є—Д—Г–ґ–љ—Л–µ –њ—А–Њ–±–Є—А–Ї–Є
вАҐ –Я–∞—Б—В–µ—А–Њ–≤—Б–Ї–Є–µ –њ–Є–њ–µ—В–Ї–Є
вАҐ –°—В–µ–Ї–ї–∞ –њ—А–µ–і–Љ–µ—В–љ—Л–µ
вАҐ –°—В–µ–Ї–ї–∞ –њ–Њ–Ї—А–Њ–≤–љ—Л–µ, # 00
вАҐ –І–∞—И–Ї–∞ –і–ї—П —Б—В–µ–Ї–Њ–ї
вАҐ –Э–Є–Ј–Ї–Њ—Б–Ї–Њ—А–Њ—Б—В–љ–∞—П —Ж–µ–љ—В—А–Є—Д—Г–≥–∞
вАҐ –Т–Њ—А—В–µ–Ї—Б-–Љ–Є–Ї—Б–µ—А
–Я—А–Њ—В–Њ–Ї–Њ–ї
1. –Т–љ–µ—Б–Є—В–µ –Ї—Г–ї—М—В—Г—А—Г –≤–Њ —Д–ї–∞–Ї–Њ–љ 75-—Б–Љ2 –њ—А–Є –њ–ї–Њ—В–љ–Њ—Б—В–Є 2—Е10*4-5—Е10*4 –Ї–ї./–Љ–ї (4—Е10*3–Є 1—Е10*4 –Ї–ї./—Б–Љ2) –≤ –Њ–±—К–µ–Љ–µ 20 –Љ–ї.
2. –Я—А–Є–±–ї–Є–Ј–Є—В–µ–ї—М–љ–Њ —З–µ—А–µ–Ј 3-5 –і–љ—П, –Ї–Њ–≥–і–∞ –Ї–ї–µ—В–Ї–Є –љ–∞—Е–Њ–і—П—В—Б—П –≤ log-—Д–∞–Ј–µ —А–Њ—Б—В–∞, –і–Њ–±–∞–≤—М—В–µ –Ї —Б—А–µ–і–µ 0,2 –Љ–ї –Ї–Њ–ї—Ж–µ–Љ–Є–і–∞ lxlO-5 –Ь –і–Њ –Ї–Њ–љ–µ—З–љ–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є1—Е107–Ь.
3. –І–µ—А–µ–Ј 4-6 —З –Њ—Б—В–Њ—А–Њ–ґ–љ–Њ —Г–і–∞–ї–Є—В–µ —Б—А–µ–і—Г, –і–Њ–±–∞–≤—М—В–µ 5 –Љ–ї 0,25% —В—А–Є–њ—Б–Є–љ–∞ –Є –Є–љ–Ї—Г–±–Є—А—Г–є—В–µ –Ї—Г–ї—М—В—Г—А—Г 10 –Љ–Є–љ.
4. –¶–µ–љ—В—А–Є—Д—Г–≥–Є—А—Г–є—В–µ –Ї–ї–µ—В–Ї–Є –≤ —В—А–Є–њ—Б–Є–љ–µ, —Г–і–∞–ї–Є—В–µ —Б—Г–њ–µ—А–љ–∞—В–∞–љ—В —Б —В—А–Є–њ—Б–Є–љ–Њ–Љ.
5. –†–µ—Б—Г—Б–њ–µ–љ–і–Є—А—Г–є—В–µ –Ї–ї–µ—В–Ї–Є –≤ 5 –Љ–ї –≥–Є–њ–Њ—В–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —А–∞—Б—В–≤–Њ—А–∞ –Є –Њ—Б—В–∞–≤—М—В–µ –Є—Е –≤ —В–µ—З–µ–љ–Є–µ 20 –Љ–Є–љ –њ—А–Є 37 ¬∞–°.
6. –Ф–Њ–±–∞–≤—М—В–µ —А–∞–≤–љ—Л–є –Њ–±—К–µ–Љ —Б–≤–µ–ґ–µ–њ—А–Є–≥–Њ—В–Њ–≤–ї–µ–љ–љ–Њ–≥–Њ —Е–Њ–ї–Њ–і–љ–Њ–≥–Њ —Г–Ї—Б—Г—Б–љ–Њ–≥–Њ –Љ–µ—В–∞–љ–Њ–ї–∞, –њ–Њ—Б—В–Њ—П–љ–љ–Њ –њ–µ—А–µ–Љ–µ—И–Є–≤–∞—П, –Ј–∞—В–µ–Љ –Њ—В—Ж–µ–љ—В—А–Є—Д—Г–≥–Є—А—Г–є—В–µ –Ї–ї–µ—В–Ї–Є –њ—А–Є 100 g –≤ —В–µ—З–µ–љ–Є–µ 2 –Љ–Є–љ.
7. –£–і–∞–ї–Є—В–µ —Б—Г–њ–µ—А–љ–∞—В–∞–љ—В, —А–∞–Ј–±–µ–є—В–µ –Њ—Б–∞–і–Њ–Ї –љ–∞ –≤–Њ—А—В–µ–Ї—Б-–Љ–Є–Ї—Б–µ—А–µ, –Љ–µ–і–ї–µ–љ–љ–Њ –і–Њ–±–∞–≤–ї—П—П —Б–≤–µ–ґ–Є–є —Г–Ї—Б—Г—Б–љ—Л–є –Љ–µ—В–∞–љ–Њ–ї –њ—А–Є –њ–Њ—Б—В–Њ—П–љ–љ–Њ–Љ –њ–µ—А–µ–Љ–µ—И–Є–≤–∞–љ–Є–Є.
8. –Ю—Б—В–∞–≤—М—В–µ –Ї–ї–µ—В–Ї–Є –≤ —В–µ—З–µ–љ–Є–µ 10 –Љ–Є–љ –љ–∞ –ї—М–і—Г.
9. –¶–µ–љ—В—А–Є—Д—Г–≥–Є—А—Г–є—В–µ –Ї–ї–µ—В–Ї–Є –≤ —В–µ—З–µ–љ–Є–µ 2 –Љ–Є–љ –њ—А–Є 100 g.
10. –£–і–∞–ї–Є—В–µ —Б—Г–њ–µ—А–љ–∞—В–∞–љ—В, —Б–Њ–і–µ—А–ґ–∞—Й–Є–є —Г–Ї—Б—Г—Б–љ—Л–є –Љ–µ—В–∞–љ–Њ–ї, –Є —А–µ—Б—Г—Б–њ–µ–љ–і–Є—А—Г–є—В–µ –Њ—Б–∞–і–Њ–Ї –љ–∞ –≤–Њ—А—В–µ–Ї—Б-–Љ–Є–Ї—Б–µ—А–µ –≤ 0,2 –Љ–ї —Г–Ї—Б—Г—Б–љ–Њ–≥–Њ –Љ–µ—В–∞–љ–Њ–ї–∞, —З—В–Њ–±—Л –њ–Њ–ї—Г—З–Є—В—М —Б—Г—Б–њ–µ–љ–Ј–Є—О –Њ—В–і–µ–ї—М–љ—Л—Е –Ї–ї–µ—В–Њ–Ї.
11. –Э–∞–±–µ—А–Є—В–µ –Њ–і–љ—Г –Ї–∞–њ–ї—О —Б—Г—Б–њ–µ–љ–Ј–Є–Є –≤ –Ї–Њ–љ—З–Є–Ї –њ–∞—Б—В–µ—А–Њ–≤—Б–Ї–Њ–є –њ–Є–њ–µ—В–Ї–Є –Є –Ї–∞–њ–љ–Є—В–µ –њ—А–Є–Љ–µ—А–љ–Њ —Б –≤—Л—Б–Њ—В—Л 30 —Б–Љ –љ–∞ —Е–Њ–ї–Њ–і–љ–Њ–µ –њ—А–µ–і–Љ–µ—В–љ–Њ–µ —Б—В–µ–Ї–ї–Њ. –Э–∞–Ї–ї–Њ–љ–Є—В–µ —Б—В–µ–Ї–ї–Њ –Є –њ–Њ–Ј–≤–Њ–ї—М—В–µ –Ї–∞–њ–ї–µ —Б—В–µ—З—М –њ–Њ —Б—В–µ–Ї–ї—Г.
12. –С—Л—Б—В—А–Њ –≤—Л—Б—Г—И–Є—В–µ —Б—В–µ–Ї–ї–Њ –љ–∞–і —Б–Њ—Б—Г–і–Њ–Љ —Б –Ї–Є–њ—П—Й–µ–є –≤–Њ–і–Њ–є, –Є—Б—Б–ї–µ–і—Г–є—В–µ –≤ —Д–∞–Ј–Њ–≤–Њ-–Ї–Њ–љ—В—А–∞—Б—В–љ–Њ–Љ –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–µ. –Х—Б–ї–Є –Ї–ї–µ—В–Ї–Є —А–∞–≤–љ–Њ–Љ–µ—А–љ–Њ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ—Л –Є –љ–µ –Ї–∞—Б–∞—О—В—Б—П –і—А—Г–≥ –і—А—Г–≥–∞, –њ—А–Є–≥–Њ—В–Њ–≤—М—В–µ –±–Њ–ї—М—И–µ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ —Б—В–µ–Ї–Њ–ї, –Є—Б–њ–Њ–ї—М–Ј—Г—П —В—Г –ґ–µ —Б–∞–Љ—Г—О –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—О –Ї–ї–µ—В–Њ–Ї. –Х—Б–ї–Є –Ї–ї–µ—В–Њ–Ї —Б–ї–Є—И–Ї–Њ–Љ –Љ–љ–Њ–≥–Њ –Є –Њ–љ–Є –њ–µ—А–µ–Ї—А—Л–≤–∞—О—В –і—А—Г–≥ –і—А—Г–≥–∞, —В–Њ –љ–∞–і–Њ —А–∞–Ј–≤–µ—Б—В–Є —Б—Г—Б–њ–µ–љ–Ј–Є—О –≤ 2 —А–∞–Ј–∞ –Є –≤ 4 —А–∞–Ј–∞ –Є –≤–љ–Њ–≤—М —Б–і–µ–ї–∞—В—М –њ—А–µ–њ–∞—А–∞—В –Ї–∞–њ–ї–Є. –Х—Б–ї–Є –Ї–ї–µ—В–Ї–Є –њ—А–Є —А–∞–Ј–≤–µ–і–µ–љ–Є–Є
–љ–∞—Е–Њ–і—П—В—Б—П –≤ —Г–і–Њ–≤–ї–µ—В–≤–Њ—А–Є—В–µ–ї—М–љ–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є, —В–њ—А–Є–≥–Њ—В–Њ–≤—М—В–µ –±–Њ–ї—М—И–µ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ —Б—В–µ–Ї–Њ–ї. –Х—Б–ї–Є –љ–µ—В, —В–Њ —А–∞–Ј–≤–µ–і–Є—В–µ —Б—Г—Б–њ–µ–љ–Ј–Є—О –і–∞–ї–µ–µ –Є –њ–Њ–≤—В–Њ—А–Є—В–µ —Н—В–Њ—В —И–∞–≥.
13.–Ю–Ї—А–∞—Б—М—В–µ –Ї–ї–µ—В–Ї–Є –Ї—А–∞—Б–Є—В–µ–ї–µ–Љ –У–Є–Љ–Ј–∞:
–∞) –†–∞–Ј–Љ–µ—Б—В–Є—В–µ —Б—В–µ–Ї–ї–∞ –≤ –Ї—О–≤–µ—В—Г –і–ї—П –Њ–Ї—А–∞—И–Є–≤–∞–љ–Є—П, –њ–Њ–Љ–µ—Й–µ–љ–љ—Г—О –љ–∞–і —А–∞–Ї–Њ–≤–Є–љ–Њ–є.
–±) –Я–Њ–ї–љ–Њ—Б—В—М—О –њ–Њ–Ї—А–Њ–є—В–µ –Ї–ї–µ—В–Ї–Є –љ–µ—Б–Ї–Њ–ї—М–Ї–Є–Љ–Є –Ї–∞–њ–ї—П–Љ–Є –њ—А–Њ—Д–Є–ї—М—В—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –Ї—А–∞—Б–Є—В–µ–ї—П –У–Є–Љ–Ј–∞ –љ–∞ 2 –Љ–Є–љ.
–≤) –Ч–∞–ї–µ–є—В–µ —Б—В–µ–Ї–ї–∞ –њ—А–Є–±–ї–Є–Ј–Є—В–µ–ї—М–љ–Њ 10-–Ї—А–∞—В–љ—Л–Љ –Њ–±—К–µ–Љ–Њ–Љ –≤–Њ–і—Л.
–≥) –Ю—Б—В–∞–≤—М—В–µ —Б—В–µ–Ї–ї–∞ –і–ї—П –і–∞–ї—М–љ–µ–є—И–µ–є –Њ–Ї—А–∞—Б–Ї–Є –µ—Й–µ –љ–∞ 2 –Љ–Є–љ.
–і) –Ю—В–Љ–Њ–є—В–µ –Ї—А–∞—Б–Є—В–µ–ї—М –њ—А–Њ—В–Њ—З–љ–Њ–є –≤–Њ–і–Њ–є.
–Я—А–Є–Љ–µ—З–∞–љ–Є–µ. –Э–µ —Б–ї–Є–≤–∞—В—М –Ї—А–∞—Б–Є—В–µ–ї—М —Б–Њ —Б—В–µ–Ї–Њ–ї, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г —Н—В–Њ –Њ—Б—В–∞–≤–Є—В –љ–∞ —Б—В–µ–љ–Ї–µ –њ–µ–љ—Г –Њ–Ї–Є—Б–ї–Є–≤—И–µ–є—Б—П –Ї—А–∞—Б–Ї–Є; –≤—Б–µ–≥–і–∞ —Б–Љ—Л–≤–∞—В—М –Ї—А–∞—Б–Є—В–µ–ї—М –≤–Њ–і–Њ–є. –Ф–∞–ґ–µ –Ї–Њ–≥–і–∞ –Њ–Ї—А–∞—И–Є–≤–∞–љ–Є–µ –њ—А–Њ–≤–Њ–і–Є—В—Б—П –≤ —З–∞—И–Ї–µ, –Ї—А–∞—Б–Є—В–µ–ї—М –љ–Є–Ї–Њ–≥–і–∞ –љ–µ —Б–ї–Є–≤–∞—О—В, –Њ–љ –і–Њ–ї–ґ–µ–љ –±—Л—В—М —Б–Љ—Л—В —Б—В—А—Г–µ–є –≤–Њ–і—Л.
–µ) –Ч–∞–Ї–Њ–љ—З–Є—В–µ –Њ–Ї—А–∞—Б–Ї—Г, –њ—А–Њ–Љ—Л–≤–∞—П –Ї–∞–ґ–і–Њ–µ —Б—В–µ–Ї–ї–Њ –њ—А–Њ—В–Њ—З–љ–Њ–є –≤–Њ–і–Њ–є, —З—В–Њ–±—Л —Г–і–∞–ї–Є—В—М –ї—О–±–Њ–є –Њ—Б–∞–і–Њ–Ї –Ї—А–∞—Б–Є—В–µ–ї—П.
–ґ) –Я—А–Њ–≤–µ—А—М—В–µ –Њ–Ї—А–∞—Б–Ї—Г –њ–Њ–і –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–Њ–Љ. –Х—Б–ї–Є –Ї–∞—З–µ—Б—В–≤–Њ —Г–і–Њ–≤–ї–µ—В–≤–Њ—А–Є—В–µ–ї—М–љ–Њ, –њ–Њ–ї–љ–Њ—Б—В—М—О –≤—Л—Б—Г—И–Є—В–µ —Б—В–µ–Ї–ї–Њ, –Ј–∞–Ї—А–Њ–є—В–µ –њ–Њ–Ї—А–Њ–≤–љ—Л–Љ —Б—В–µ–Ї–ї–Њ–Љ #* 00 –њ—А–Є –њ–Њ–Љ–Њ—Й–Є –Ї–ї–µ—П DPX –Є–ї–Є Permount.
|