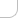–Ь–Ш–Ъ–†–Ю–°–Ъ–Ю–Я–Ш–ѓ –Т –Ґ–Х–Ь–Э–Ю–Ь –Я–Ю–Ы–Х
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ –≤ —В–µ–Љ–љ–Њ–Љ –њ–Њ–ї–µ (—В–µ–Љ–љ–Њ–њ–Њ–ї—М–љ–∞—П –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–Є—П) –Њ—Б–љ–Њ–≤–∞–љ–Њ –љ–∞ —П–≤–ї–µ–љ–Є—П—Е —А–∞—Б—Б–µ—П–љ–Є—П —Б–≤–µ—В–∞ –њ—А–Є —Б–Є–ї—М–љ–Њ–Љ –±–Њ–Ї–Њ–≤–Њ–Љ –Њ—Б–≤–µ—Й–µ–љ–Є–Є –≤–Ј–≤–µ—И–µ–љ–љ—Л—Е –≤ –ґ–Є–і–Ї–Њ—Б—В–Є —З–∞—Б—В–Є—Ж. –Ь–Є–Ї—А–Њ—Б–Ї–Њ–њ–Є—П –≤ —В–µ–Љ–љ–Њ–Љ –њ–Њ–ї–µ –Ј—А–µ–љ–Є—П –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Г–≤–Є–і–µ—В—М –±–Њ–ї–µ–µ –Љ–µ–ї–Ї–Є–µ —З–∞—Б—В–Є—Ж—Л, —З–µ–Љ –≤ —Б–≤–µ—В–Њ–≤–Њ–Љ –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–µ. –Ю–љ–∞ –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–µ—В—Б—П —Б –њ–Њ–Љ–Њ—Й—М—О –Њ–±—Л—З–љ–Њ–≥–Њ —Б–≤–µ—В–Њ–≤–Њ–≥–Њ –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–∞, —Б–љ–∞–±–ґ–µ–љ–љ–Њ–≥–Њ —Б–њ–µ—Ж–Є–∞–ї—М–љ—Л–Љ–Є –Ї–Њ–љ–і–µ–љ—Б–Њ—А–∞–Љ–Є (–њ–∞—А–∞–±–Њ–ї–Њ–Є–і- –Ї–Њ–љ–і–µ–љ—Б–Њ—А –Ю–Ш-10 –Є–ї–Є –Ї–∞—А–і–Є–Њ–Є–і-–Ї–Њ–љ–і–µ–љ—Б–Њ—А –Ю–Ш-13) , –Ї–Њ—В–Њ—А—Л–є —Б–Њ–Ј–і–∞–µ—В –њ–Њ–ї—Л–є –Ї–Њ–љ—Г—Б —Б–≤–µ—В–∞. –Т–µ—А—И–Є–љ–∞ —Н—В–Њ–≥–Њ –њ–Њ–ї–Њ–≥–Њ –Ї–Њ–љ—Г—Б–∞ —Б–Њ–≤–њ–∞–і–∞–µ—В —Б –Њ–±—К–µ–Ї—В–Њ–Љ. –Ы—Г—З–Є —Б–≤–µ—В–∞, –њ—А–Њ—Е–Њ–і—П —З–µ—А–µ–Ј –Њ–±—К–µ–Ї—В –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤ –Ї–Њ—Б–Њ–Љ –љ–∞–њ—А–∞–≤–ї–µ–љ–Є–Є, –љ–µ –њ–Њ–њ–∞–і–∞—О—В –≤ –Њ–±—К–µ–Ї—В–Є–≤ –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–∞. –Т –љ–µ–≥–Њ –њ—А–Њ–љ–Є–Ї–∞–µ—В —В–Њ–ї—М–Ї–Њ —Б–≤–µ—В, —А–∞—Б—Б–µ—П–љ–љ—Л–є –Њ–±—К–µ–Ї—В–Њ–Љ.
 
–Я—А–Є —Н—В–Њ–Љ –љ–∞ —В–µ–Љ–љ–Њ–Љ —Д–Њ–љ–µ –љ–∞–±–ї—О–і–∞—О—В—Б—П —П—А–Ї–Њ —Б–≤–µ—В—П—Й–Є–µ—Б—П –Ї–Њ–љ—В—Г—А—Л –Љ–Є–Ї—А–Њ–±–љ—Л—Е –Ї–ї–µ—В–Њ–Ї –Є –і—А—Г–≥–Є—Е —З–∞—Б—В–Є—Ж. –Ь–Є–Ї—А–Њ—Б–Ї–Њ–њ–Є—П –≤ —В–µ–Љ–љ–Њ–Љ –њ–Њ–ї–µ –Ј—А–µ–љ–Є—П –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Њ–њ—А–µ–і–µ–ї–Є—В—М —Д–Њ—А–Љ—Г –Љ–Є–Ї—А–Њ–±–∞ –Є –µ–≥–Њ –њ–Њ–і–≤–Є–ґ–љ–Њ—Б—В—М. –Ю–±—Л—З–љ–Њ —В–µ–Љ–љ–Њ–њ–Њ–ї—М–љ–∞—П –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–Є—П –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –њ—А–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ —Б–ї–∞–±–Њ –њ–Њ–≥–ї–Њ—Й–∞—О—В —Б–≤–µ—В –Є –љ–µ –≤–Є–і–љ—Л –≤ —Б–≤–µ—В–Њ–≤–Њ–Љ –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–µ, –Ї–∞–Ї, –љ–∞–њ—А–Є–Љ–µ—А, —Б–њ–Є—А–Њ—Е–µ—В—Л.
–Ф–ї—П —Б–Њ–Ј–і–∞–љ–Є—П —В–µ–Љ–љ–Њ–≥–Њ –њ–Њ–ї—П –Љ–Њ–ґ–љ–Њ —В–∞–Ї–ґ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –Њ–±—Л—З–љ—Л–є –Ї–Њ–љ–і–µ–љ—Б–Њ—А –Р–±–±–µ, –њ–Њ–Љ–µ—Б—В–Є–≤ –≤ —Ж–µ–љ—В—А –µ–≥–Њ –Ї—А—Г–ґ–Њ–Ї —З–µ—А–љ–Њ–є –±—Г–Љ–∞–≥–Є. –Т —Н—В–Њ–Љ —Б–ї—Г—З–∞–µ —Б–≤–µ—В —Г—Б—В–∞–љ–∞–≤–ї–Є–≤–∞—О—В –Є —Ж–µ–љ—В—А–Є—А—Г—О—В –њ–Њ —Б–≤–µ—В–Њ–≤–Њ–Љ—Г –њ–Њ–ї—О, –∞ –Ј–∞—В–µ–Љ –Ј–∞—В–µ–Љ–љ—П—О—В –Ї–Њ–љ–і–µ–љ—Б–Њ—А –Р–±–±–µ.
–Я—А–µ–њ–∞—А–∞—В –і–ї—П –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–Є–Є –≥–Њ—В–Њ–≤—П—В –њ–Њ –Љ–µ—В–Њ–і—Г —А–∞–Ј–і–∞–≤–ї–µ–љ–љ–Њ–є –Ї–∞–њ–ї–Є. –Ґ–Њ–ї—Й–Є–љ–∞ –њ—А–µ–і–Љ–µ—В–љ–Њ–≥–Њ —Б—В–µ–Ї–ї–∞ –љ–µ –і–Њ–ї–ґ–љ–∞ –њ—А–µ–≤—Л—И–∞—В—М 1 вАФ1,1 –Љ–Љ, –Є–љ–∞—З–µ —Д–Њ–Ї—Г—Б –Ї–Њ–љ–і–µ–љ—Б–Њ—А–∞ –њ—А–Є–і–µ—В—Б—П –≤ —В–Њ–ї—Й—Г —Б—В–µ–Ї–ї–∞. –Ь–µ–ґ–і—Г –Ї–Њ–љ–і–µ–љ—Б–Њ—А–Њ–Љ –Є –њ—А–µ–і–Љ–µ—В–љ—Л–Љ —Б—В–µ–Ї–ї–Њ–Љ –њ–Њ–Љ–µ—Й–∞—О—В –ґ–Є–і–Ї–Њ—Б—В—М (–і–Є—Б—В–Є–ї–ї–Є—А–Њ–≤–∞–љ–љ–∞—П –≤–Њ–і–∞) —Б –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–Љ –њ—А–µ–ї–Њ–Љ–ї–µ–љ–Є—П, –±–ї–Є–Ј–Ї–Є–Љ –Ї –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—О –њ—А–µ–ї–Њ–Љ–ї–µ–љ–Є—П —Б—В–µ–Ї–ї–∞. –Я—А–Є –њ—А–∞–≤–Є–ї—М–љ–Њ–є —Г—Б—В–∞–љ–Њ–≤–Ї–µ –Њ—Б–≤–µ—Й–µ–љ–Є—П –љ–∞ —В–µ–Љ–љ–Њ–Љ –њ–Њ–ї–µ –≤–Є–і–љ—Л —П—А–Ї–Є–µ, —Б–≤–µ—В—П—Й–Є–µ—Б—П —В–Њ—З–Ї–Є.
–Ф—А—Г–≥–Њ–µ –Њ–≥—А–∞–љ–Є—З–µ–љ–Є–µ –Љ–µ—В–Њ–і–∞ —В–µ–Љ–љ–Њ–њ–Њ–ї—М–љ–Њ–є –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–Є–Є —Б–Њ—Б—В–Њ–Є—В –≤ —В–Њ–Љ, —З—В–Њ –≤ –њ–Њ–ї–µ –Ј—А–µ–љ–Є—П –Њ–Ї–∞–Ј—Л–≤–∞–µ—В—Б—П —Б–ї–Є—И–Ї–Њ–Љ –Љ–љ–Њ–≥–Њ –і–µ—В–∞–ї–µ–є, —В–∞–Ї–Є—Е, –Ї–∞–Ї –њ—Г–Ј—Л—А—М–Ї–Є –≤–Њ–Ј–і—Г—Е–∞ –Є–ї–Є –Є–љ–Њ—А–Њ–і–љ—Л–µ —З–∞—Б—В–Є—Ж—Л, –Ї–Њ—В–Њ—А—Л–µ —Г—Е—Г–і—И–∞—О—В –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–µ.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –і–∞–љ–љ—Л–є –Љ–µ—В–Њ–і –ї—Г—З—И–µ –≤—Б–µ–≥–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –і–ї—П –Є–Ј—Г—З–µ–љ–Є—П –Љ–µ–ї–Ї–Є—Е –і–Є—Б–Ї—А–µ—В–љ—Л—Е —Б—В—А—Г–Ї—В—Г—А, –і–Њ—Б—В–∞—В–Њ—З–љ–Њ —Г–і–∞–ї–µ–љ–љ—Л—Е –і—А—Г–≥ –Њ—В –і—А—Г–≥–∞.
–Ъ–Њ–љ–і–µ–љ—Б–Њ—А —Б–≤–µ—В–ї–Њ–≥–Њ –Є —В–µ–Љ–љ–Њ–≥–Њ –њ–Њ–ї—П –Ю–Ш-10
–Ъ–Њ–љ–і–µ–љ—Б–Њ—А –Ю–Ш-10 –њ—А–µ–і–љ–∞–Ј–љ–∞—З–∞–µ—В—Б—П —Б–Њ–Ј–і–∞–љ–Є—П –≤ –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–µ —Б–≤–µ—В–ї–Њ–≥–Њ –Є —В–µ–Љ–љ–Њ–≥–Њ –њ–Њ–ї—П –њ—А–Є –Њ—Б–≤–µ—Й–µ–љ–Є–Є –Њ–±—К–µ–Ї—В–Њ–≤ –њ—А–Њ—Е–Њ–і—П—Й–Є–Љ —Б–≤–µ—В–Њ–Љ. –Ъ–Њ–љ–і–µ–љ—Б–Њ—А –≤—Б—В–∞–≤–ї—П–µ—В—Б—П –≤ –≥–Є–ї—М–Ј—Г –Њ—Б–≤–µ—В–Є—В–µ–ї—М–љ–Њ–≥–Њ —Б—В–Њ–ї–Є–Ї–∞ –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–∞ –љ–∞ –Љ–µ—Б—В–Њ –Њ–±—Л—З–љ–Њ–≥–Њ –Ї–Њ–љ–і–µ–љ—Б–Њ—А–∞.
–Р–њ–µ—А—В—Г—А–∞ –Ї–Њ–љ–і–µ–љ—Б–Њ—А–∞ —Б–≤–µ—В–ї–Њ–≥–Њ –њ–Њ–ї—П 0,6
–Р–њ–µ—А—В—Г—А–∞ –Ї–Њ–љ–і–µ–љ—Б–Њ—А–∞ —В–µ–Љ–љ–Њ–≥–Њ –њ–Њ–ї—П 0,7

–Ъ–Њ–љ–і–µ–љ—Б–Њ—А —В–µ–Љ–љ–Њ–≥–Њ –њ–Њ–ї—П –Ю–Ш-13
–Ґ–Х–•–Э–Ш–І–Х–°–Ъ–Ю–Х –Ю–Я–Ш–°–Р–Э–Ш–Х –Ш –Ш–Э–°–Ґ–†–£–Ъ–¶–Ш–ѓ –Я–Ю –≠–Ъ–°–Я–Ы–£–Р–Ґ–Р–¶–Ш–Ш
–Ъ–Њ–љ–і–µ–љ—Б–Њ—А —В–µ–Љ–љ–Њ–≥–Њ –њ–Њ–ї—П –Ю–Ш-13 (–Ї–∞—А–і–Є–Њ–Є–і) –њ—А–µ–і–љ–∞–Ј–љ–∞—З–∞–µ—В—Б—П –і–ї—П –Њ—Б–≤–µ—Й–µ–љ–Є—П –Њ–±—К–µ–Ї—В–Њ–≤ –њ—А–Њ—Е–Њ–і—П—Й–Є–Љ —Б–≤–µ—В–Њ–Љ –њ–Њ –Љ–µ—В–Њ–і—Г —В–µ–Љ–љ–Њ–≥–Њ –њ–Њ–ї—П –њ—А–Є —А–∞–±–Њ—В–µ —Б –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–∞–Љ–Є —Б–µ—А–Є–Є ¬Ђ–С–Є–Њ–ї–∞–Љ¬ї. –Р–њ–µ—А—В—Г—А–∞ –Ї–Њ–љ–і–µ–љ—Б–Њ—А–∞ ... 1,2. –†–∞—Б—Б—В–Њ—П–љ–Є–µ –Њ—В –њ–Њ—Б–ї–µ–і–љ–µ–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є —Д—А–Њ–љ—В–∞–ї—М–љ–Њ–є –ї–Є–љ–Ј—Л –Ї–Њ–љ–і–µ–љ—Б–Њ—А–∞ –і–Њ –њ–ї–Њ—Б–Ї–Њ—Б—В–Є –њ—А–µ–і–Љ–µ—В–∞ (—Б —Г—З–µ—В–Њ–Љ —Е–Њ–і–∞ –ї—Г—З–µ–є –≤ —Б—В–µ–Ї–ї–µ –Є –Є–Љ–Љ–µ—А—Б–Є–Њ–љ–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є) ... –Њ—В 1,25 –і–Њ 1,4 –Љ–Љ.
–Ь–µ—В–Њ–і —В–µ–Љ–љ–Њ–≥–Њ –њ–Њ–ї—П –њ—А–Є–Љ–µ–љ—П–µ—В—Б—П –і–ї—П –њ–Њ–ї—Г—З–µ–љ–Є—П –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П –њ—А–Њ–Ј—А–∞—З–љ—Л—Е, –љ–µ–њ–Њ–≥–ї–Њ—Й–∞—О—Й–Є—Е –Є –њ–Њ—В–Њ–Љ—Г –љ–µ –≤–Є–і–Є–Љ—Л—Е –њ—А–Є –љ–∞–±–ї—О–і–µ–љ–Є–Є –≤ —Б–≤–µ—В–ї–Њ–Љ –њ–Њ–ї–µ –Њ–±—К–µ–Ї—В–Њ–≤. –Я—Г—З–Њ–Ї –ї—Г—З–µ–є, –Њ—Б–≤–µ—Й–∞—О—Й–Є—Е –Њ–±—К–µ–Ї—В, –≤—Л—Е–Њ–і–Є—В –Є–Ј –Ї–Њ–љ–і–µ–љ—Б–Њ—А–∞ –≤ –≤–Є–і–µ –њ–Њ–ї–Њ–≥–Њ –Ї–Њ–љ—Г—Б–∞ –Є –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ –≤ –Њ–±—К–µ–Ї—В–Є–≤ –љ–µ –њ–Њ–њ–∞–і–∞–µ—В. –Ш–Ј–Њ–±—А–∞–ґ–µ–љ–Є–µ —Б–Њ–Ј–і–∞–µ—В—Б—П —В–Њ–ї—М–Ї–Њ —Б–≤–µ—В–Њ–Љ, –Ї–Њ—В–Њ—А—Л–є —А–∞—Б—Б–µ–Є–≤–∞–µ—В—Б—П –Љ–µ–ї–Ї–Њ—Б—В—А—Г–Ї—В—Г—А–љ—Л–Љ–Є —Н–ї–µ–Љ–µ–љ—В–∞–Љ–Є –Њ–±—К–µ–Ї—В–∞. –Т –њ–Њ–ї–µ –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–∞ –љ–∞ —В–µ–Љ–љ–Њ–Љ —Д–Њ–љ–µ –≤–Є–і–љ—Л —Б–≤–µ—В–ї—Л–µ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П –Љ–µ–ї–Ї–Є—Е –і–µ—В–∞–ї–µ–є; —Г –Ї—А—Г–њ–љ—Л—Е –і–µ—В–∞–ї–µ–є –≤–Є–і–љ—Л —В–Њ–ї—М–Ї–Њ —Б–≤–µ—В–ї—Л–µ –Ї—А–∞—П, –Ї–Њ—В–Њ—А—Л–µ —А–∞—Б—Б–µ–Є–≤–∞—О—В –Њ—Б–≤–µ—Й–∞—О—Й–Є–µ –ї—Г—З–Є.
–Ю–њ—В–Є—З–µ—Б–Ї—Г—О —Б–Є—Б—В–µ–Љ—Г –Ї–Њ–љ–і–µ–љ—Б–Њ—А–∞ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Њ—В—Ж–µ–љ—В—А–Є—А–Њ–≤–∞—В—М –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –Њ–±—К–µ–Ї—В–Є–≤–∞ –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–∞ —В–∞–Ї, —З—В–Њ–±—Л –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –≤—Л—Е–Њ–і–љ–Њ–Љ –Ј—А–∞—З–Ї–µ –Њ–±—К–µ–Ї—В–Є–≤–∞ –љ–µ –±—Л–ї–Њ –Ј–∞–Љ–µ—В–љ–Њ —Б–≤–µ—В–∞.
–Ъ–Њ–љ–і–µ–љ—Б–Њ—А —А–∞—Б—Б—З–Є—В–∞–љ –љ–∞ —А–∞–±–Њ—В—Г —Б –њ—А–µ–і–Љ–µ—В–љ—Л–Љ —Б—В–µ–Ї–ї–Њ–Љ —В–Њ–ї—Й–Є–љ–Њ–є –љ–µ –±–Њ–ї–µ–µ 1,2 –Љ–Љ. –Ъ–Њ–љ–і–µ–љ—Б–Њ—А —Б–Њ—Б—В–Њ–Є—В –Є–Ј —Б—Д–µ—А–Є—З–µ—Б–Ї–Њ–≥–Њ –Ј–µ—А–Ї–∞–ї–∞ (—А–Є—Б. 1) –Є –ї–Є–љ–Ј—Л-–Ї–∞—А–і–Є–Њ–Є–і—Л 2, —Б–Ї–ї–µ–µ–љ–љ—Л—Е –Љ–µ–ґ–і—Г —Б–Њ–±–Њ–є –Є –≤—Б—В–∞–≤–ї–µ–љ–љ—Л—Е –≤ –Њ–њ—А–∞–≤—Г 3 (—А–Є—Б. 2), –≤–≤–µ—А–љ—Г—В—Г—О –≤ —Ж–Є–ї–Є–љ–і—А 4. –¶–Є–ї–Є–љ–і—А —Г–Ї—А–µ–њ–ї–µ–љ –љ–∞ –Ї–Њ–ї—М—Ж–µ –≤–љ—Г—В—А–Є –Ї–Њ—А–њ—Г—Б–∞ 5 –Ї–Њ–љ–і–µ–љ—Б–Њ—А–∞.
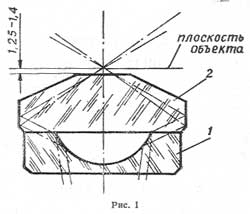 
–Ъ–Њ–љ–і–µ–љ—Б–Њ—А —Б–љ–∞–±–ґ–µ–љ –њ—А—Г–ґ–Є–љ—П—Й–Є–Љ —Г–њ—А—Г–≥–Є–Љ –Є –і–≤—Г–Љ—П —Ж–µ–љ—В—А–Є—А–Њ–≤–Њ—З–љ—Л–Љ–Є –≤–Є–љ—В–∞–Љ–Є 6.
–Э–∞ –Ї–∞–ґ–і–Њ–Љ –Ї–Њ–љ–і–µ–љ—Б–Њ—А–µ –љ–∞–≥—А–∞–≤–Є—А–Њ–≤–∞–љ—Л –µ–≥–Њ —И–Є—Д—А, –∞–њ–µ—А—В—Г—А–∞ (–Р =1,2), —В–Њ–≤–∞—А–љ—Л–є –Ј–љ–∞–Ї –њ—А–µ–і–њ—А–Є—П—В–Є—П-–Є–Ј–≥–Њ—В–Њ–≤–Є—В–µ–ї—П –Є –њ–Њ—А—П–і–Ї–Њ–≤—Л–є –љ–Њ–Љ–µ—А, –і–≤–µ –њ–µ—А–≤—Л–µ —Ж–Є—Д—А—Л –Ї–Њ—В–Њ—А–Њ–≥–Њ –Њ–Ј–љ–∞—З–∞—О—В –і–≤–µ –њ–Њ—Б–ї–µ–і–љ–Є–µ —Ж–Є—Д—А—Л –≥–Њ–і–∞ –≤—Л–њ—Г—Б–Ї–∞ –Ї–Њ–љ–і–µ–љ—Б–Њ—А–∞.
–Я–Ю–†–ѓ–Ф–Ю–Ъ –†–Р–С–Ю–Ґ–Ђ
1. –Т—Б—В–∞–≤—М—В–µ –≤ —В—Г–±—Г—Б –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–∞ –Њ–Ї—Г–ї—П—А, –≤ —А–µ–≤–Њ–ї—М–≤–µ—А –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–∞ –≤–≤–µ—А–љ–Є—В–µ –Њ–±—К–µ–Ї—В–Є–≤, –≤—Л–±—А–∞–љ–љ—Л–µ –і–ї—П –љ–∞–±–ї—О–і–µ–љ–Є—П.
2. –Э–∞—Б—В—А–Њ–є—В–µ –Њ—Б–≤–µ—Й–µ–љ–Є–µ, —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤—Г—П—Б—М —В–µ—Е–љ–Є—З–µ—Б–Ї–Є–Љ–Є –Њ–њ–Є—Б–∞–љ–Є—П–Љ–Є –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–∞ –Є –≤—Л–±—А–∞–љ–љ–Њ–≥–Њ –Њ—Б–≤–µ—В–Є—В–µ–ї—П (—А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –њ—А–Є–Љ–µ–љ—П—В—М –Њ—Б–≤–µ—В–Є—В–µ–ї–Є –Ю–Ш-19, –Ю–Ш-24, –Ю–Ш-31, –Ю–Ш-32, –Ю–Ш-36).
3. –£—Б—В–∞–љ–Њ–≤–Є—В–µ –љ–∞ –Љ–µ—Б—В–Њ –Њ–±—Л—З–љ–Њ–≥–Њ –Ї–Њ–љ–і–µ–љ—Б–Њ—А–∞ –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–∞ –Ї–Њ–љ–і–µ–љ—Б–Њ—А —В–µ–Љ–љ–Њ–≥–Њ –њ–Њ–ї—П –Є –Ј–∞–Ї—А–µ–њ–Є—В–µ –µ–≥–Њ —Б—В–Њ–њ–Њ—А–љ—Л–Љ –≤–Є–љ—В–Њ–Љ.
4. –Э–∞–љ–µ—Б–Є—В–µ –љ–∞ –≤–µ—А—Е–љ—О—О –ї–Є–љ–Ј—Г –Ї–Њ–љ–і–µ–љ—Б–Њ—А–∞ –Ї–∞–њ–ї—О –Є–Љ–Љ–µ—А—Б–Є–Њ–љ–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є.
5. –£—Б—В–∞–љ–Њ–≤–Є—В–µ –љ–∞ –њ—А–µ–і–Љ–µ—В–љ—Л–є —Б—В–Њ–ї–Є–Ї –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–∞ –њ—А–µ–њ–∞—А–∞—В –Є –Ј–∞–Ї—А–µ–њ–Є—В–µ –µ–≥–Њ. –†–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –њ—А–Є–Љ–µ–љ—П—В—М –њ—А–µ–і–Љ–µ—В–љ—Л–µ —Б—В–µ–Ї–ї–∞ —В–Њ–ї—Й–Є–љ–Њ–є –і–Њ 1,2 –Љ–Љ.
6. –Я–Њ–і–љ–Є–Љ–Є—В–µ –Ї–Њ–љ–і–µ–љ—Б–Њ—А —В–∞–Ї, —З—В–Њ–±—Л –Є–Љ–Љ–µ—А—Б–Є–Њ–љ–љ–∞—П –ґ–Є–і–Ї–Њ—Б—В—М —Б–Њ–њ—А–Є–Ї–Њ—Б–љ—Г–ї–∞—Б—М —Б –њ—А–µ–і–Љ–µ—В–љ—Л–Љ —Б—В–µ–Ї–ї–Њ–Љ –Є —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–Є–ї–∞—Б—М –њ–Њ –љ–µ–Љ—Г, –њ–Њ—Б–ї–µ —З–µ–≥–Њ —Б—Д–Њ–Ї—Г—Б–Є—А—Г–є—В–µ –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ –љ–∞ –Њ–±—К–µ–Ї—В, –њ—А–Є —Н—В–Њ–Љ –≤ –њ–Њ–ї–µ –Ј—А–µ–љ–Є—П –і–Њ–ї–ґ–µ–љ –љ–∞–±–ї—О–і–∞—В—М—Б—П —Н—Д—Д–µ–Ї—В —В–µ–Љ–љ–Њ–≥–Њ –њ–Њ–ї—П (—П—А–Ї–Њ —Б–≤–µ—В—П—Й–Є–µ—Б—П —З–∞—Б—В–Є—Ж—Л –Њ–±—К–µ–Ї—В–∞ –љ–∞ —В–µ–Љ–љ–Њ–Љ —Д–Њ–љ–µ).
7. –Я—А–Є–≤–µ–і–Є—В–µ —Б –њ–Њ–Љ–Њ—Й—М—О –≤–Є–љ—В–Њ–≤ 6 —Ж–µ–љ—В—А –Ј–Њ–љ—Л —Б —В–µ–Љ–љ–Њ–њ–Њ–ї—М–љ—Л–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ –≤ —Ж–µ–љ—В—А –њ–Њ–ї—П –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–∞ –Є –њ—А–Є—Б—В—Г–њ–Є—В–µ –Ї –љ–∞–±–ї—О–і–µ–љ–Є—О.
–Я–Њ–Љ–љ–Є—В–µ, —З—В–Њ –њ–Њ–ї—Г—З–Є—В—М —Е–Њ—А–Њ—И–Є–є —Н—Д—Д–µ–Ї—В —В–µ–Љ–љ–Њ–≥–Њ –њ–Њ–ї—П –Љ–Њ–ґ–љ–Њ —В–Њ–ї—М–Ї–Њ –њ—А–Є –њ—А–∞–≤–Є–ї—М–љ–Њ–є –љ–∞—Б—В—А–Њ–є–Ї–µ –Њ—Б–≤–µ—Й–µ–љ–Є—П.
–Я—А–Є —А–∞–±–Њ—В–µ —Б –Є–Љ–Љ–µ—А—Б–Є–Њ–љ–љ—Л–Љ–Є –Њ–±—К–µ–Ї—В–Є–≤–∞–Љ–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —Б–љ–Є–Ј–Є—В—М –Є—Е –∞–њ–µ—А—В—Г—А—Г –і–Њ 0,8 –≤ –њ—А–Њ—В–Є–≤–љ–Њ–Љ —Б–ї—Г—З–∞–µ –≤ –Њ–±—К–µ–Ї—В–Є–≤ –±—Г–і–µ—В –њ–Њ–њ–∞–і–∞—В—М –љ–µ —В–Њ–ї—М–Ї–Њ —Б–≤–µ—В, —А–∞—Б—Б–µ—П–љ–љ—Л–є —З–∞—Б—В–Є—Ж–∞–Љ–Є –Њ–±—К–µ–Ї—В–∞, –љ–Њ –Є –њ—А—П–Љ—Л–µ –ї—Г—З–Є, —Б–Њ–Ј–і–∞—О—Й–Є–µ —Б–≤–µ—В–ї—Л–є —Д–Њ–љ, —З—В–Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г—Е—Г–і—И–Є—В –Ї–Њ–љ—В—А–∞—Б—В–љ–Њ—Б—В—М –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П. –Я–Њ—Н—В–Њ–Љ—Г –њ—А–Є –љ–∞–±–ї—О–і–µ–љ–Є–Є –≤ —В–µ–Љ–љ–Њ–Љ –њ–Њ–ї–µ —Б –Њ–±—К–µ–Ї—В–Є–≤–Њ–Љ 90X1,25 —Б–ї–µ–і—Г–µ—В –њ–Њ–Љ–µ—Б—В–Є—В—М –≤ –≤—Л—Е–Њ–і–љ–Њ–є –Ј—А–∞—З–Њ–Ї –Њ–±—К–µ–Ї—В–Є–≤–∞ –і–Є–∞—Д—А–∞–≥–Љ—Г, –≤—Е–Њ–і—П—Й—Г—О –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—В –Ї–Њ–љ–і–µ–љ—Б–Њ—А–∞.
|